Cho vào mỗi bình dung dịch chứa 1 mol HCl thấy cân thăng bằng. Cho 21 gam Mg vào bình (1), cho 21 gam Fe vào bình (2). Sau khi các phản ứng xảy ra hoàn toàn, cần phải cho vào đĩa cân nào vật nặng bao nhiêu gam để cân lại thăng bằng?
A. Cho vào đĩa cân chứa bình (2): 0,25g
B. Cho vào đĩa cân chứa bình (1): 1,0g.C. Cho vào đĩa cân chứa bình (2): 1,0g
D. Cho vào đĩa cân chứa bình (1): 0,25g
Giải thích dùm mình nha!!!

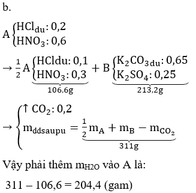
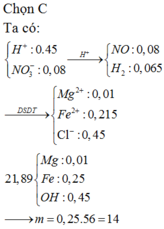
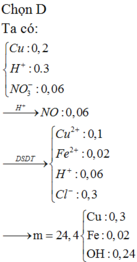
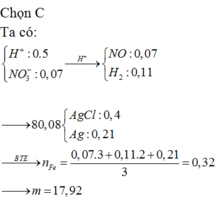
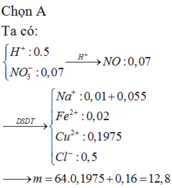

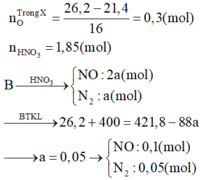

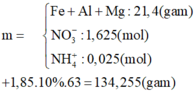
(1) \(n_{Mg}=0,875\left(mol\right)\) nên Mg dư
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,5_____1_____________0,5
\(m=21+36,5-0,5.2=56,5\left(g\right)\)
(2) \(n_{Fe}=0,375\left(mol\right)\) nên HCl dư
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,375__0,75_________0,375
\(m=21+36,5-0,375.2=56,75\left(g\right)\)
Để (1) và (2) cân bằng ,cần làm (1) tăng m thêm 0,25(g) hoặc giảm m (2) bớt 0,25 (g)
Vậy chọn D