người ta thực hiện phản ứng tổng hợp NH3 từ 3 mol N2 và 6 mol H2 .Sau phản ứng thu được 25,5 g NH3
a) tính số mol hỗn hợp khí sau phản ứng ?
b) tính hiệu suất của phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(N_2+3H_2\leftrightarrow2NH_3\\ n_{NH_3}=a\left(mol\right)\\ n_{sau}=14=9-\dfrac{1}{2}a+6-\dfrac{3}{2}a+a\\ a=1\\ n_{N_2}:1>n_{H_2}:3\\ H=\dfrac{1}{\dfrac{2}{3}.6}.100\%=25\%\)

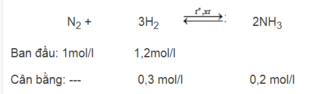
Theo PTHH thì 1 mol N 2 cần 3 mol H 2 . Ở đây chỉ có 1,2 mol H 2 , vì H 2 thiếu nên tác dụng hết. Hiệu suất phải tính theo lượng chất tác dụng hết. Số mol H 2 đã tác dụng là 0,3 mol.
Vậy h = (0,3 : 1,2). 100 = 25
Đáp số : h = 25%.

Gọi số mol \(N_2\) phản ứng là \(a\left(mol\right)\)
- Phương trình : \(N_2+3H_2\rightarrow2NH_3\)
Trước phản ứng: 9 6
Phản ứng : \(a\) \(3a\) \(2a\)
Dư: \(\left(9-a\right)\)\(\left(6-3a\right)\) \(2a\)
− Theo bài ra : \(\left(9-a\right)+\left(6-3a\right)+2a=14\)
\(\rightarrow15-2a=14\Rightarrow a=0,5\)
Hiệu suất phản ứng:
\(H=\dfrac{0,5}{9}.100\%=5,56\%\)

Sau phản ứng áp suất của hệ giảm 10% mà tỉ lệ về số mol cũng chính là tỉ lệ về áp suất
⇒ Tổng số mol khí sau phản ứng giảm 10% so với ban đầu
⇒ Số mol khí sau = 90% số mol khí ban đầu
Giả sử a =1⇒ Ban đầu có 1 mol N2 và 3 mol H2
N2 + 3H2 → 2NH3
Bđ: 1 3 (mol)
Pư:x 3x 2x
Tổng số mol khí sao phản ứng là: 4 – 2x
⇒ 4 – 2x = 90%.4 = 3,6 ⇒ x = 0,2
⇒ H = 20%
Đáp án C.
\(n_{hhspu}=\frac{25,5}{17}=1,5\left(mol\right)\)
\(PTHH:N_2+3H_2\underrightarrow{t^o,xt}2NH_3\)
(mol)_____1______3_______2
(mol)_____2/3____2_________4/3
Tỉ lệ: 3/1 > 6/3 => N2 dư
\(H=\frac{\frac{4}{3}}{1,5}.100=88,9\left(\%\right)\)
Ta có :
\(\text{ nNH3=1.5}\)
.................\(\text{ N2+2H2-->2NH3}\)
trươc..............3........6................
phản ứng........0.75.....1.5..........1.5
sau ...............2.25......4.5....1,5
\(\text{a. Số mol khí sau phản ứng=2.25+4.5+1.5=8.25}\)
b. Ta có \(\frac{3}{1}=\frac{6}{2}\)
=>Ta có thể tính hiệu suất theo N2 hoặc H2
\(\Rightarrow\text{H=0.75/3=25%}\)