Nguyên tử X có 3 đồng vị \(^{^A1}X\) chiếm 92,3%; \(^{^A2}X\) chiếm 4,7% còn lại là đồng vị thứ 3. Tổng khối lượng của 3 đồng vị là 87, tổng khối lượng của 200 nguyên tử là 5621,4. Mặt khác số nơtron trong đồng vị 2 nhiều trong đồng vị 1 là 1 đồng vị
a) Tìm số khối của 3 đồng vị
b) Biết trong đồng vị 1 có số p=số n. Tìm số nơtron của 3 đồng vị.

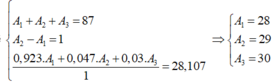
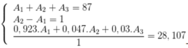
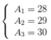
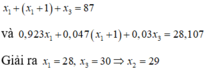
%A3 = 100% - 92,3% - 4,7% = 3 %
Ta có : A1 + A2 + A3 = 87 (I)
Trong 200 nguyên tử có :
Số nguyên tử của đồng vị A1 là : \(\frac{200\cdot92,3\%}{100\%}\)~185 (nguyên tử )
số nguyên tử của đồng vị A2 là : \(\frac{200\cdot4,7\%}{100\%}\) ~ 9 ( nguyên tử )
số nguyên tử của đồng vị A3 là : 00 - 185 - 9 = 6 (nguyên tử )
ta có : 185A1 + 9A2 + 6A3 = 5621,4 (II)
Mà : N2 = N1 + 1
<=> A2 = A1 + 1 <=> -A1 + A2 = 1 (III)
Giair hệ phương trình (I) , (II) và (III) ta được
A1 ~ 28
A2 ~ 29
A3 ~ 30
b, Ta có : P1 = N1 mà A1 = P1 + N1 = 28
<=> P1 + P1 = 28
<=> P2 = P3 = N1 = P1 = 14
Số nơ tron trong đồng vị A1 là 14 (hạt)
Số nơ tron trong đồng vị A2 là 29 - 14 = 15 hạt
Số nơ tron trong đồng vị A3 là 30 - 14 = 16 hạt