Hòa tan hoàn toàn m gam hỗn hợp A gồm Mg và MgCO3 bằng dung dịch H2SO4 loãng, dư thu được 6,72 lit hỗn hợp khí (ở điều kiện tiêu chuẩn). Dẫn từ từ hỗn hợp khí này qua bình chứa 300ml dung dịch NaOH 1M để phản ứng xảy ra hoàn toàn thu được dung dịch B. Cô cạn cẩn thận dung dịch B để nước bay hơi hết thu được 14,6 gam chất rắn.Tính m

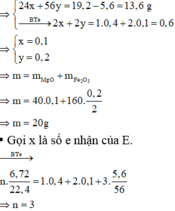

Hỗn hợp khí thu được gồm H2 và CO2 có tổng mol = 6,72/22,4= 0,3 mol
----> nCO2 < 0,3 mol
hỗn hợp khí cho vào NaOH chỉ có CO2 phản ứng
nNaOH/nCO2 > 1 (vì nCO2 < 0,3) --> dung dịch B có 2 khả năng:
TH1: B gồm 2 muối NaHCO3 và Na2CO3 ; NaOH hết
Gọi nNa2CO3=x ; nNaHCO3 = 0,3-2x
-> m=106x + (0,3-2x).84= 14,6 --> x=0,171 ( loại vì nNa2CO3 = 0,171.2=0,342 > nNaOH)
TH2. B gồm Na2CO3 và NaOH dư
Gọi nCO2= x --> nNa2CO3=x -> nNaOH= 0,3-2x
m=106x + (0,3-2x).40 = 14,6
--> x= 0,1 mol ---> nCO2=0,1 mol ; nH2= 0,2 mol
--> nMg= 0,2 ; nMgCO3 = 0,1
--> m=0,2.24 + 0,1.84= 13,2 g
hh khí: CO2 + H2
n (hh khí) = 6,72 : 22,4 =0,3 =>nCO2 < 0,3
n(NaOH b.đ)= 300 x 0,001 x1 =0,3
Do n(NaOH b.đ) > nCO2 => s.p tạo thành sẽ là NaCO3 (NaOH có thể dư) theo cơ chế:
NaOH + CO2 ----> NaHCO3
sau đó:
NaHCO3 + NaOH ----> Na2CO3 + H2O
Đặt x = nNaOH(dư), y = nNa2CO3
{40x + 106y = 14,6 (khối lượng rắn)
{x + 2y = 0,3 (mol Na ko thay đổi)
=> x= 0,1, y=0,1
y=0,1 =>nC (trong Na2CO3)= 0,1 => nCO2 = 0,1
=>nCO2 =0,1; nH2 = 0,2
nCO2 = 0,1 => nMgCO3 = 0,1
nH2 = 0,2 => nMg =0,2