Cho 100ml dung dịch MgCl2 2M tác dụng 150ml Ba(OH)2 2,5M thu được dung dịch A có D=1,12g/ml tính c% các chất trong dung dịch
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(n_{HCl}=Cm.V=1.0,1=1mol\)
\(n_{H_2SO_4}=Cm.V=0,5.0,1=0,05mol\)
Thể thích của dd D là 200ml = 0,2l
\([H^+]=\frac{n_{HCl}+2.n_{H_2SO_4}}{V}=\frac{0,1+0,1}{0,2}=1M\)
\([Cl^-]=\frac{n_{HCl}}{V}=\frac{0,1}{0,2}=0,5M\)
\([SO_4^{2-}]=\frac{n_{H_2SO_4}}{V}=\frac{0,05}{0,2}=0,25M\)
Khi cho dd D vào \(Ba\left(OH\right)_2\) chỉ có \(H_2SO_4\) tác dụng, tạo kết tủa
\(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2H_2O\)
\(0,05....\rightarrow0,05mol\)
\(\rightarrow m_{BaSO_4}=n.M=0,05.233=11,65g\)

\(n_{MgCl_2}\)=\(0,1.2=0,2(mol)\)
\(n_{Ba(OH)_2}\)=\(0,15.1,5=0,225(mol) \)
\({MgCl_2}+{Ba(OH)_2}-->{Mg(OH)_2}+{BaCl_2}\)
Dung dịch A chứa 0,225-0,2=0,025 mol \({Ba(OH)_2}\) dư; 0,2 mol \({BaCl_2}\)
Kết tủa B là 0,2 mol \({Mg(OH)_2}\)
\({Mg(OH)_2}-->MgO+{H_2O}\)
⇒\(n_{MgO}\)=\(n_{Mg(OH)_2}=0,2 mol\)
⇒\(m_{MgO}=0,2.40=8(g)\)
Coi thể tích dung dịch không đổi sau khi trộn
\(V_{dd}=100+150=250ml=0,25l\)
⇒\(C_M{Ba(OH)_2}\)=\(\dfrac{0,025}{0,25}=0,1M\)
\(C_M{BaCl_2}=\dfrac{0,2}{0,25}=0,8M\)
mdd(sau phản ứng)=250.1,12=280(g)
C%\({Ba(OH)_2}=\dfrac{0,025.171}{280}.100=1,5%\)%
C%\({BaCl_2}=\dfrac{0,2.208}{280}.100=14,85%\)%

\(a)n_{BaCl_2}=\dfrac{240}{1,12}:1000\cdot1=\dfrac{3}{14}mol\\ n_{H_2SO_4}=\dfrac{122.20}{100}:98=\dfrac{61}{245}mol\\ BaCl_2+H_2SO_4\rightarrow BaSO_4+2HCl\\ \Rightarrow\dfrac{3:14}{1}< \dfrac{61:245}{1}\Rightarrow H_2SO_4.dư\\ n_{BaSO_4}=n_{BaCl_2}=n_{H_2SO_4}=\dfrac{3}{14}mol\\ m_{kt}=m_{BaSO_4}=\dfrac{3}{14}\cdot233=50g\\ c)C_{\%H_2SO_4\left(dư\right)}=\dfrac{\left(61:245-3:14\right)98}{240+122-50}\cdot100=1,2\%\)

Gọi: \(\left\{{}\begin{matrix}n_{FeCl_3}=x\left(mol\right)\\n_{MgCl_2}=y\left(mol\right)\end{matrix}\right.\)
PT: \(FeCl_3+3KOH\rightarrow Fe\left(OH\right)_{3\downarrow}+3KCl\)
______x_________3x_________x (mol)
\(MgCl_2+2KOH\rightarrow Mg\left(OH\right)_{2\downarrow}+2KCl\)
____y_________2y_________y (mol)
Ta có: \(n_{KOH}=0,2.2,5=0,5\left(mol\right)\)
⇒ 3x + 2y = 0,5 (1)
m kết tủa = 16,5 ⇒ 107x + 58y = 16,5 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
\(\Rightarrow C_{M_{FeCl_3}}=C_{M_{MgCl_2}}=\dfrac{0,1}{0,5}=0,2\left(M\right)\)
\(FeCl_3+3KOH\rightarrow Fe\left(OH\right)_3\downarrow+3KCl\\ MgCl_2+2KOH\rightarrow Mg\left(OH\right)_2\downarrow+2KCl\)
\(n_{KOH}=0,2\cdot2,5=0,5\left(mol\right)\)
Đặt nFeCl₃ trong 500ml X là a mol, nMgCl₂ trong 500ml X là b mol
\(\Rightarrow\left\{{}\begin{matrix}3a+2b=0,5\\107a+58b=16,5\end{matrix}\right.\\ \Leftrightarrow\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(\Rightarrow C_MFeCl_3=\dfrac{0,1}{0,5}=0,2\left(M\right)\\ C_MMgCl_2=\dfrac{0,1}{0,5}=0,2\left(M\right)\)

\(n_{HCl}=0,1.1=0,1\left(mol\right)\)
\(n_{Ba\left(OH\right)_2}=0,1.1=0,1\left(mol\right)\)
PTHH :
\(2HCl+Ba\left(OH\right)_2\rightarrow BaCl_2+2H_2O\)
trc p/u : 0,1 0,1
p/u : 0,1 0,05 0,05 0,1
sau p/u : 0 0,05 0,05 0,1
\(C_{M_{BaCl_2}}=\dfrac{0,05}{0,2}=0,25\left(M\right)\)
\(C_{M_{Ba\left(OH\right)_2dư}}=\dfrac{0,05}{0,2}=0,25\left(M\right)\)
\(m_{BaCl_2}=0,05.208=10,4\left(g\right)\)

2.
a)
+nFe2(SO4)3 = 0.1*2 = 0.2 (mol)
+nBa(OH)2 = 0.15*1.5 = 0.225 (mol)
3Ba(OH)2 + Fe2(SO4)3 => 2Fe(OH)3↓ + 3BaSO4↓(1)
0.225...................0.2.................
2Fe(OH)3(t*) => Fe2O3 + 3H2O(2)
0.15.........................0.075...........
_Dựa vào phương trình (1) ta thấy Fe2(SO4)3 còn dư 0.125 mol => dd(B) : Fe2(SO4)3
Fe2(SO4)3 + 3BaCl2 => 3BaSO4↓ + 2FeCl3
0.125..................0.375............0.375
b)
_Chất rắn (D) : Fe2O3 và BaSO4 không bị phân hủy.
=>m(D) = mFe2O3 + mBaSO4 = 0.075*160 + 0.375*233 = 99.375(g)
_Chất rắn (E) : BaSO4
=>m(E) = mBaSO4 = 0.375*233 = 87.375(g)
c)
_Dung dịch (B) : Fe2(SO4)3
=>Vdd(sau) = 150 + 100 = 250 (ml) = 0.25 (lit)
=>nFe2(SO4)3 (dư) = 0.125 (mol)
=>CM(Fe2(SO4)3) = 0.125 / 0.25 = 0.5 (M)

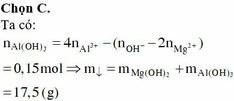
MgCl2 + Ba(OH)2 => Mg(OH)2| + BaCl2
nMgCl2 = CM.V = 0.2 (mol)
nBa(OH)2 = CM.V = 2.5 x 0.15 = 0.375 (mol)
Lập tỉ số: 0.2/1 < 0.375/1 => MgCl2 hết, Ba(OH)2 dư
mBaCl2 = n.M = 0.2 x 208 = 41.6 (g)
mBa(OH)2 dư = (0.375-0.2)x171 = 29.925 (g)
V dd sau pứ = 100 + 150 = 250ml dd
m dd sau pứ = D.V = 1.12 x 250 = 280 (g)
C% dd BaCl2 = 14.857%
C% dd Ba(OH)2 dư = 10.6875%