Sản xuất H2SO4 theo sơ đồ sau :
\(S\rightarrow SO_2\rightarrow SO_3\rightarrow H_2SO_4\)
Tính khối lượng quặng lưu huỳnh chứa 60% lưu huỳnh để sản xuất 2 tấn H2SO4 . Biết hiệu suất đạt 80%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng dung dịch H 2 SO 4 50% thu được :
100 tấn dung dịch có 50 tấn H 2 SO 4
x tấn ← 73,5 tấn
x = 73,5x100/50 = 147 tấn

a) 4FeS2 + 11O2 ––> 2Fe2O3 + 8SO2
2SO2 + O2 -----(tº)------> 2SO3
SO3 + H2O ––> H2SO4
Trên thực tế, SO3 cũng bị hấp thụ bởi H2SO4 để tạo ra ôleum (H2S2O7), chất này sau đó bị làm loãng để tạo thành axít sulfuric.
H2SO4 + SO3 → H2S2O7
Ôleum sau đó phản ứng với nước để tạo H2SO4 đậm đặc.
H2S2O7+ H2O → 2 H2SO4
b) 1.2 tấn= 1200000g
mFeS2= 1200000*90%=1080000g
=>nFeS2=1080000/120=9000 mol
Ta có sơ đồ : FeS2 ---> 2SO2 -->2SO3 --> 2H2SO4
9000 mol 18000 mol
Theo định luật bảo toàn nguyên tố:
nH2SO4= 18000*85%=15300 mol
=>mH2SO4= 15300*98= 1499400g
Theo đề C%= 96%
=>mddH2SO4=1499400*100/96=1561875g=1.561875 tấn
Số khủng khiếp quá, bạn xem lại giúp tôi nhé. tôi tính hơi nhanh :)

Fe + S (0,04 mol) \(\underrightarrow{t^o}\) FeS (0,04 mol).
Số mol sắt (II) sunfua cần sản xuất là 3,52/88=0,04 (mol).
Khối lượng lưu huỳnh cần dùng trên lý thuyết là 0,04.32=1,28 (g).
Khối lượng quặng lưu huỳnh thực tế cần dùng là 1,28:90%:90%=128/81 (g).

Khối lượng lưu huỳnh chứa trong 80 tấn quặng:
m S = 80x40/100 = 32 tấn
Điều chế H 2 SO 4 theo sơ đồ sau
S → SO 2 → SO 3 → H 2 SO 4
Ta thấy: Cứ 32g S thì sản xuất được 98g H 2 SO 4
⇒ m H 2 SO 4 = 32x98/32 = 98 tấn
Hiệu ứng phản ứng: H = 73,5/98 x 100 = 75%

a)\(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\)
\(2SO_2+O_2\underrightarrow{t^o}2SO_3\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
b)\(m_{H_2SO_4}=\dfrac{50\cdot49\%}{100\%}=24,5g\Rightarrow n_{H_2SO_4}=0,25mol\)
Từ quá trình trên: \(4FeS_2\rightarrow H_2SO_4\)
\(\Rightarrow n_{FeS_2}=\dfrac{1}{4}n_{H_2SO_4}=\dfrac{1}{4}\cdot0,25=\dfrac{1}{16}mol\)\
\(m_{FeS_2}=\dfrac{1}{16}\cdot120=7,5g\)
c)\(n_{NaOH}=0,3\cdot1=0,3mol\)
\(SO_2+2NaOH\rightarrow Na_2SO_3+H_2O\)
0,15 0,3 0,15
\(m_{Na_2SO_3}=0,15\cdot126=18,9g\)

Đáp án C.
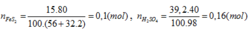
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

Đề có phải là : ' Từ 80 tấn quặng Pirit chứa 40% lưu huỳnh , người ta sản xuất được 73,5 tấn axit sunfuric . '' đúng không
nH2SO4=2/98=1/49 (mol)
\(S\rightarrow SO_2\rightarrow SO_3\rightarrow H_2SO_4\)
\(\frac{1}{49}\) \(\frac{1}{49}\)
mS=\(\frac{1}{49}.32=\frac{32}{49}\)
m S (thực có) = \(\frac{32}{49}.\frac{100}{80}=\frac{40}{49}\)
mquặng S=\(\frac{40}{49}.\frac{100}{60}=1,36\left(tấn\right)\)