Khi cho nhôm tác dụng với axit sunfuric, khối lượng của nhôm sunfat tạo thành nhỏ hơn nhôm cộng với khối lượng đã tham gia phản ứng . Hãy giải thích xem kết quả trên có phù hợp với định luật bảo toàn khối lượng ko
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
Định Luật Bảo toàn khối lượng :
\(m_{Al}+m_{H_2SO_4}=m_{Al_2\left(SO_4\right)_3}+m_{H_2}\)
\(\Rightarrow m_{H_2}=2.7+14.7-17.1=0.3\left(g\right)\)
\(n_{H_2}=\dfrac{0.3}{2}=0.15\left(mol\right)\)
\(V_{H_2}=0.15\cdot22.4=3.36\left(l\right)\)

a: \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
b: \(n_{H2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(\Leftrightarrow n_{Al}=0.1\left(mol\right)\)
\(m_{Al}=n_{Al}\cdot M_{Al}=0.1\cdot27=2.7\left(g\right)\)

Theo định luật bảo toàn khối lượng ta có: mMg + mHCl = mMgCl2 + mH2
Điều này có phù hợp với định luật bảo toàn khối lượng vì khí cho Mg tác dụng với HCl sinh ra dung dịch MgCl2 và khí H2. Khí H2 sinh ra sẽ bay lên và dung dịch còn lại chỉ còn MgCl2

a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\)
Vậy \(Al\left(OH\right)_3\) dư.
\(m_{dư}=0,75.78-98.0,5=9,5\left(g\right)\)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)

a, \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right);n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
PTHH: 2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
Mol: \(\dfrac{1}{3}\) 0,5 \(\dfrac{1}{6}\)
b, Ta có: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\) ⇒ Al(OH)3 dư, H2SO4 hết
⇒ \(m_{Al\left(OH\right)_3}=\left(0,75-\dfrac{1}{3}\right).78=32,5\left(g\right)\)
c, \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Không có chất dư (hoặc có thể bn cho sai 49(g) dung dịch là 49(g) H2SO4)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al\left(OH\right)_3}=\dfrac{1}{2}.0,75=0,375\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,375.342=128,25\left(g\right)\)

\(\left(a\right)2Al+3H_2O\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ \left(b\right)n_{H_2}=\dfrac{13,44}{22,4}=0,6mol\\ n_{Al}=\dfrac{0,6.2}{3}=0,4mol\\ m_{Al}=0,4.27=10,8g\\ \left(c\right)n_{O_2}=\dfrac{4,8}{32}=0,15mol\\ 4Al+3O_2\underrightarrow{t^0}2Al_2O_3\\ \Rightarrow\dfrac{0,4}{4}>\dfrac{0,15}{3}\Rightarrow Al.dư\\ n_{Al_2O_3}=\dfrac{0,15.2}{3}=0,1mol\\ m_{oxit}=m_{Al_2O_3}=0,1.102=10,2g\)
a: \(2Al+3H_2SO_4\rightarrow1Al_2\left(SO_4\right)_3+3H_2\uparrow\)
0,4 0,6 0,2 0,6
b: \(n_{H_2}=\dfrac{13.44}{22.4}=0.6\left(mol\right)\)
=>\(n_{Al}=0.4\left(mol\right)\)
\(m_{Al}=0.4\cdot27=10.8\left(g\right)\)
c: \(4Al+3O_2\rightarrow2Al_2O_3\)
0,4 0,2
\(m_{Al_2O_3}=0.2\left(27\cdot2+16\cdot3\right)=0.2\cdot102=20.4\left(g\right)\)

Phương trình hóa học của phản ứng:
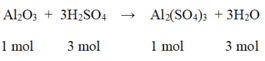
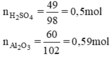
So sánh tỉ lệ 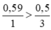 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
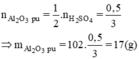
mAl2O3 (dư) = 60 - 17 = 43(g)
mk chưa hiểu đề cho lắm
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
Theo đề bài: \(m_{Al_2\left(SO_4\right)_3}< m_{Al}+m_{H_2SO_4}\)
Theo định luật bào toàn: \(m_{Al}+m_{H_2SO_4}\) luôn bằng \(m_{Al_2\left(SO_4\right)_3}+m_{H_2}\)
\(\Rightarrow m_{Al_2\left(SO_4\right)_3}< m_{Al}+m_{H_2SO_4}\)
Vậy kết quả đề bài trên phù hợp với định luật bảo toàn khối lượng