Thành phần chính của cát, thuỷ tinh là hợp chất giữa Si và O. Trong hợp chất này, người ta xác định được rằng nguyên tố silic (Si) chiếm 46,67% về khối lượng. Viết công thức hoá học và tính khối lượng mol phân tử của hợp chất.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Gọi công thức của hợp chất là S i x H y .
Theo đề bài ta có:
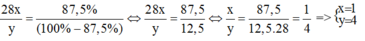
CTHH của hợp chất là S i H 4 .
Phân tử khối là: 28 + 4.1 = 32 ( đvC)

Câu 16 :
a) CTHH : $SiH_n$
Ta có : $\%Si = \dfrac{28}{28 + n}.100\% = 87,5\% \Rightarrow n = 4$
Vậy CTHH là $SiH_4$
$PTK = 32(đvC)$
b) Si có hóa trị IV trong hợp chất
Câu 17 :
a) Gọi CTHH là $Fe_xO_y$
Ta có : $\dfrac{56x}{7} = \dfrac{16y}{3} \Rightarrow \dfrac{x}{y} = \dfrac{2}{3}$
Vậy oxit là $Fe_2O_3$
PTK = 160 đvC
b) Fe có hóa trị III trong hợp chất
Câu 18 :
$X_2(SO_4)_3 \Rightarrow $ X có hóa trị III
$H_3Y \Rightarrow $ Y có hóa trị III
Theo quy tắc hóa trị, CTHH cần tìm là XY
Câu 19 :
a) CTHH : $T_2O_3$
$\%T = \dfrac{2T}{2T + 16.3}.100\% = 53\%$
$\Rightarrow T = 27(Al)$
Vậy T là nhôm
b) CTHH là $Al_2O_3$
$PTK = 102(đvC)$
Câu 20 :
a) CTHH là $H_3XO_y$
Ta có : $M_A = 3 + X + 16y = 98(1)$
$\%O = \dfrac{16y}{98}.100\% = 61,31\%(2)$
Từ (1)(2) suy ra X = 31 ; y = 4
b)
X là Photphot, kí hiệu P

a)
gọi hợp chất đó là x
\(d_{X/O_2}=\dfrac{M_x}{M_{O_2}}=\dfrac{M_X}{32}=0,5\\ =>M_X=0,5\cdot32=16\left(\dfrac{g}{mol}\right)\)
nguyên tố Cacbon chiếm: 100%-25%=75%
\(m_C=\dfrac{16\cdot75}{100}=12\left(g\right);m_H=\dfrac{16\cdot25}{100}=4\left(g\right)\)
\(n_C=\dfrac{12}{12}=1\left(mol\right);n_H=\dfrac{4}{1}=4\left(mol\right)\)
=> 1 phân tử hợp chất có có 1 nguyên tử C, 4 nguyên tử H
=> CTHH: CH4
b)
\(M_{Cu\left(OH\right)_2}=64+\left(16+1\right)\cdot2=98\left(\dfrac{g}{mol}\right)\)
\(\%m_{Cu}=\dfrac{64\cdot100}{98}=65,3\%\)
\(\%m_O=\dfrac{\left(16\cdot2\right)\cdot100}{98}=32,7\%\)
\(\%m_H=100\%-32,7\%-65,3\%=2\%\)
Gọi CTHH của hợp chất khí là CxHy
Ta có: dCxHyH2=MCxHyMH2=MCxHy2=15dCxHyH2=MCxHyMH2=MCxHy2=15
⇒MCxHy=15×2=30(g)⇒MCxHy=15×2=30(g)
Ta có: %MC=12x30=80100⇒x=30×80100÷12=2%MC=12x30=80100⇒x=30×80100÷12=2
Vậy x=2x=2
Ta có: 12×2+1×y=3012×2+1×y=30
⇔24+y=30⇔24+y=30
⇔y=6⇔y=6
Vậy CTHH của hợp chất khí là C2H6

a, Gọi công thức của hợp chất Si và H là SixHy(x,y nguyên dương)
%H=100%-87,5%=12,5%
Ta có tỉ lệ:x:y=%Si/M(Si) : %H/M(H)
=87,5/28:12,5/1
=3,125:12.5
=1:4
=>CT:SiH4
PTK(SiH4)=28+4=32
b,Gọi hóa trị của Si là a(a nguyên dương)
Aps dụng quy tắc hóa trị: a*1=I*4
=>a=IV
=>hóa trị cuiar Silic trong hợp chất là 4

\(Gọi:\\ A:N_xO_y\\ x:y=\dfrac{7}{14}:\dfrac{12}{16}=0,5:0,75=2:5\\ A:N_2O_5\\ M_A=14\cdot2+16\cdot5=108\)
Đề hỏi PTK nếu em kí hiệu như vậy là sai rồi em

Gọi CTHH của hợp chất là TxOy
Theo quy tắc hóa trị ta có :
III.x=II.y \(\Rightarrow\frac{x}{y}=\frac{II}{III}=\frac{2}{3}\)
Vậy CTHH của hợp chất là T2O3
Ta có : T chiếm 53% nên O chiếm 47%
Ta lại có:
\(x:y=\frac{\text{%T}}{M_T}:\frac{\%O}{M_O}=\frac{53}{M_T}:\frac{47}{16}\)
\(\Leftrightarrow\frac{2}{3}=\frac{53}{M_T}:\frac{47}{16}=\frac{53}{M_T}.\frac{16}{47}\)
\(\Rightarrow M_T=\frac{3.53.16}{2.47}\approx27\)
Vậy T là nhôm. KHHH : Al
\(\Rightarrow\) CTHH của hợp chất là Al2O3
Phân tử khối của Al2O3 = 27.2+16.3 = 102(đvC)
Gọi CTHH là $Si_xO_y$
$\%O = 100\% -46,67\% = 53,33\%$
Ta có :
\(\dfrac{28x}{46,67}=\dfrac{16y}{53,33}\Rightarrow\dfrac{x}{y}=0,5=\dfrac{1}{2}\)
Vậy CTHH cần tìm là $SiO_2$
$M_{SiO_2} = 60(đvC)$
%O=100-46,67=53,33%
=>Si:O=46,67.28\100:53,33.16\100=1:2
=>SiO2
M SiO2=28+16.2=60đvC