Thí nghiệm 1
cách làm : lấy một ít lưu huỳnh cho vào muôi đốt hóa chất, đốt trên ngọc lửa đèn cồn, quan sát cháy trong không khí, sau đó đưa nhanh vào bình đựng khí oxi
nêu hiện tượng quan sát được, so sánh mức độ cháy của lưu huỳnh trong không khí và của lưu huỳnh trong không khí và của lưu huỳnh trong oxi
viết PTHH của phản ứng xảy ra trong thí nghiệm trên , biết rằng khi lưu huỳnh (S) cháy trong trong oxi( O\(_2\) tạo thành khí lưu huỳnh đioxit( SO2 ) (còn gọi là khí sunfurơ) và còn rất ít lưu huỳnh trioxit


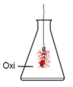
Chất rắn dần dần chuyển thành chất khí mùi độc(SO2)
Khi cháy thì lưu huỳnh cháy ở trong oxi mãnh liệt hơn trong kk
S + O2 \(\underrightarrow{t^o}SO_2\)
2SO2 + O2 \(\underrightarrow{t^o}\)2SO3
Ta có PTHH \(S+O_2\underrightarrow{t^0}SO_2\)
Hiện tượng : Lưu huỳnh cháy sáng