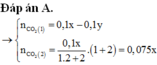X là dung dịch hcl nồng độ x mol/lít, y là dung dịch na2co3 nồng độ y mol/lít. Nhỏ từ từ 100ml dd X vào 100ml dd Y thu được V1 lít khí co2 ở đktc. Nhỏ từ từ 100ml dd Y vào 100ml dd X thu được V2 lít khí co2 ở đktc. Biết tỉ lệ V1:V2 = 4: 7. Tỉ lệ x:y là?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C
Trường hợp 1: Khi nhỏ từ từ axit vào dung dịch muối cacbonat, phản ứng xảy ra theo trình từ
H+ + CO32- → HCO3-
Sau đó H+còn dư + HCO3- → CO2 + H2O
=> nCO2 = nH+ – nCO32- = 0,1(x – y)
Trường hợp 2: Khi nhỏ từ từ muối cacbonat vào axit thì phản ứng tạo ra ngay CO2:
2H+ + CO32- → CO2 + H2O
nCO2 = ½ nH+ = 0,05x
Do V1 : V2 = 4 : 7
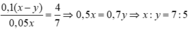

Trường hợp 1: Khi nhỏ từ từ axit vào dung dịch muối cacbonat, phản ứng xảy ra theo trình từ
H+ + CO32- → HCO3-
Sau đó H+còn dư + HCO3- → CO2 + H2O
→ nCO2 = nH+ – nCO32- = 0,1(x – y)
Trường hợp 2: Khi nhỏ từ từ muối cacbonat vào axit thì phản ứng tạo ra ngay CO2:
2H+ + CO32- → CO2 + H2O
nCO2 = ½ nH+ = 0,05x
Do V1 : V2 = 4 : 7
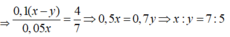
Đáp án C

Chọn C.
T N 1 : n H + = n C O 3 2 - + n C O 2 ( T N 1 ) 0 , 1 x 0 , 1 y ? T N 2 : n H + = 2 n C O 3 2 - p ư = 2 n C O 2 ( T N 2 ) 0 , 1 x ? ? ⇒ n C O 2 ( T N 1 ) = 0 , 1 x - 0 , 1 y n C O 2 ( T N 2 ) = 0 , 05 x ⇒ 0 , 1 x - 0 , 1 y 0 , 05 x = 4 7 ⇒ x y = 7 5

Chọn đáp án B
Chú ý : Khi cho HCl vào C O 3 2 - thì
![]()
Nhưng khi cho C O 3 2 - vào HCl thì
![]()
+ Ta có :
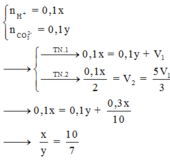

Gọi thể tích của dung dịch HCl là V(lít)
Các phản ứng
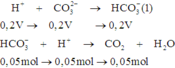
Sau phản ứng cho nước vôi trong dư vào dung dịch Y thì được kết tủa
Trong dung dịch Y còn chứa anion H C O 3 - ⇒ H+ phản ứng hết.
Sau (1), (2) có n H C O 3 - còn lại = 0,2V – 0,05 + 0,1 = 0,2V + 0,05
Khi cho nước vôi trong vào dung dịch Y ta có phản ứng sau:
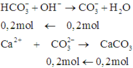
Do đó, ta có 0,2V + 0,05 = 0,2 mol ⇒ V = 0,75
Tổng số mol HCl là: 0,2V + 0,05 = 0,2 . 0,75 + 0,05 = 0,2 mol
Nồng độ của HCl: C M = n v = 0 , 2 0 , 2 = 1 M
Đáp án C.

+ Tính các giá trị đã biết:
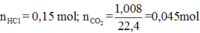
+ Với bài toán tổng hợp như này, thì ta phải viết các phương trình cụ thể cho dễ quan sát:
(1) H+ + CO3- ⟶ HCO3-
(2) H+ + HCO3- ⟶ CO2 +H2O.
Vì thu được khí CO2 nên có xảy ra phản ứng (2) ⇒ CO32- đã phản ứng hết với H+.
+ Từ
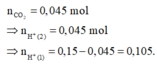
+ Vì khi thêm dung dịch Ba(OH)2 vào dung dịch Y thu được kết tủa nên trong Y phải có muối HCO3-
Như vậy suy ra ngay HCl đã phản ứng hết
Do đó từ (1) và (2) ta suy ra
![]()
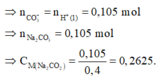
Loại ngay các đáp án A và B.
Việc cần thực hiện bây giờ là đi tính nồng độ của KHCO3 trong dung dịch X:
Vậy dung dịch Y chỉ chứa các ion K+, Na+, HCO3- và Cl-.
+ Khi thêm dịch Ba(OH)2 dư vào dung dịch Y thì:
![]()
Sau đó thì
![]()
+ Do đó 29,55 gam kết tủa là BaCO3:
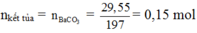
Ta sử dụng Bảo toàn nguyên tố C, toàn bộ C trong dung dịch Y chuyển hóa hết về trong kết tủa (vì thêm dung dịch Ba(OH)2 dư vào):
![]()
+ Lại áp dụng bảo toàn nguyên tốC ta được:
![]()
Hay ![]()
![]()
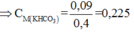
Đáp án D

Chọn đáp án A
Do VCO2 ở 2 thí nghiệm khác nhau ⇒ HCl không dư || nHCl = 0,1x; nCO32– = 0,1y mol; nHCO3– = 0,2y mol.
Thí nghiệm 1: nCO2 = nH+ - nCO32– = 0,1x - 0,1y
Thí nghiệm 2: do ban đầu nHCO3– = 2.nCO32– ⇒ nHCO3– phản ứng = 2.nCO32–phản ứng
⇒ nCO32–phản ứng = 0,1x ÷ (2 + 2 × 1) = 0,025x ⇒ nHCO3– phản ứng = 0,05x ⇒ nCO2 = 0,025x + 0,05x = 0,075x
⇒ 0,075x = 2 × (0,1x - 0,1y) ⇒ 0,125x = 0,2y ⇒ x : y = 8 : 5 ⇒ chọn A.