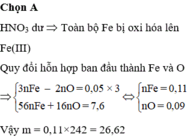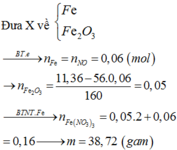cho 11.36 gam hỗn hợp gồm fe feo fe2o3 fe3o4 phản ứng hêt với h2so4 đặc nóng dư thì thu được 2.016 lít so2là thuốc khử duy nhất và dung dịch X. Khô cạn dung dịch X thu được m g muối than. tính m
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Ta có, nFe = 0,225 mol và nSO2 = 0,1875 mol
Quy hỗn hỗn hợp X về 2 nguyên tố Fe và O
Quá trình nhường: Fe0 → Fe+3 + 3e
Quá trình nhận e: O0 + 2e → O-2
S+6 + 2e → S+4
Áp dụng định luật bảo toàn electron ta có:
0,675 = 2x + 0,375 → x = 0,15
Mặt khác ta có: nên: m = 12,6 + 0,15.16 = 15 (gam).

\(n_{NO}=\dfrac{0,672}{22,4}=0,03mol\)
\(\Rightarrow n_{HNO_3}=4n_{NO}=4\cdot0,03=0,12mol\)
\(\Rightarrow n_{NO_3^-}=0,12mol\)
\(m_{muối}=m_{kl}+62n_{NO_3^-}=5,68+62\cdot0,12=13,12g\)
\(n_{NO}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\)
Quy đổi hỗn hợp X về Fe (x mol) và O (y mol)
Ta có: mX = mFe + mO → 56x + 16y = 5,68 (1)
Các quá trình trao đổi electron:
\(\overset{0}{Fe}\rightarrow\overset{+3}{Fe}+3e\)
\(\overset{0}{O}+2e\rightarrow\overset{-2}{O}\)
\(\overset{+5}{N}+3e\rightarrow\overset{+2}{N}\)
Áp dụng bảo toàn electron: \(3n_{Fe}=2n_O+3n_{NO}\)
\(\Rightarrow3x=2y+3.0,03\rightarrow3x-2y=0,09\left(2\right)\)
Từ (1) và (2) → x = 0,08; y = 0,075
Bảo toàn nguyên tố Fe:
\(nFe\left(NO_3\right)_3=n_{Fe}=0,08\left(mol\right)\)
→ m muối = 0,08.242 = 19,36 gam

Định hướng tư duy giải
→ n NH 4 + = 0 , 235 . 2 - 0 , 14 . 3 8 = 0 , 00625
=> 110,23 = 0,73943m + 96.(0,235+0,26057m/16) => m = 38,07
=> mY = 28,15 + 62.(0,00625.8 + 0,14.3 + 0,62.2) + 80.0,00625 = 134,67

Quy đổi hỗn hợp thành hỗn hợp Fe (a mol) và O (b mol) =>56a + 16b = 11,36
Bảo toàn electron
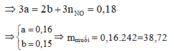
Đáp án D

Coi như hỗn hợp gồm Fe, FeO, Fe2O3, Fe3O4 gồm có x mol Fe và y mol O
Ta có 56x+16y= 11,36 (1)
Ta có nNO= 0,06 mol
QT cho e :
Fe → Fe3++ 3e
x 3x mol
QT nhận e :
O+ 2e→ O-2
y 2y mol
N+5+ 3e → NO
0,18←0,06
Theo ĐL BT electron thì : ne cho= ne nhận nên 3x= 2y+ 0,18 (2)
Từ (1) và (2) ta có x= 0,16 và y= 0,15
Bảo toàn nguyên tố Fe có nFe(NO3)3= nFe= x= 0,16 mol→ mFe(NO3)3=38,72 gam
Đáp án D

Đáp án A
Quy hỗn hợp X về dạng Fe và O.
=> mX = 56nFe + 16nO = 14,4g (1)
- Khi X + H2SO4: Bảo toàn e: 3nFe = 2nO + 2nSO2
=> 3nFe – 2nO = 2.6,72: 22,4 = 0,6 mol (2)
Từ (1,2) => nFe = 0,24; nO = 0,06 mol
Vậy muối trong dung dịch sau phản ứng sẽ là: 0,12 mol Fe2(SO4)3
=> mFe2(SO4)3 = 0,12.400 = 48g