cần dùng bao nhiêu tấn quặng pirit chứa 85% FeS2 để sản xuất 0,98 tấn H2SO4 nguyên chất biết hiệu suất của quá trình là 80%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án C.
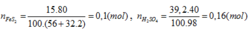
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%

ôi t làm nhầm....kq là
3,8 tấn ( cân bằng thêm 2 vào h2so4 là okok)
FeS2 ==> H2SO4
120g 98g
2,85( vì 5% tạp chất) 2,3275 (tấn)
vì H=80% ====> m H2SO4=1,3965( tấn). nhưng có C% H2SO4= 98%
VẬY mdd H2S04 là 1,425 tấn

\(m_{H_2SO_4}=\dfrac{1000000.98\%}{100\%}=980000(g)\\ \Rightarrow n_{H_2SO_4}=\dfrac{980000}{98}=10000(mol)\\ \Rightarrow n_{FeS_2}=\dfrac{1}{2}n_{H_2SO_4}.80\%=4000(mol)\\ \Rightarrow m_{FeS_2}=4000.120=480000(g)\)

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.

Quặng này chứa 10% tạp chất trơ tức
FeS2 chiếm 90%.
Vậy khối lượng quặng pirit sắt cần:
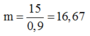

Đáp án A
Để đơn giản về tính toán thì ta xem đơn vị tấn như gam.



Bạn ơi. Cái mFes2 =0.6 tấn là thực tế. Mình phải tìm mFeS2 lí thuyết rồi mới nhân cho 100 chia 85 chứ? :"))