hh A gồm O2 , O3 có tỉ khối so với H2 = 19,2 hh B gồm ch4, c2h2 có tỉ khối với He = 5.5. tính thể tích A cần để đốt cháy 5,6l B
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


ta có dhh/H2=6--->Mtrung bình hỗ hợp khí =6*2=12
bạn dùng sơ đồ đường chéo mk làm mẫu phần a kau còn lại tương tự nha
nN2 (28) 12-2=10
nH2 (2) 12 28-12=16 ta có % thể tich = % về sô mol ----> %Vh2=\(\frac{16}{10+16}\)=61,5 %( xấp xỉ nha) %VN2 = 100-61,5=38,5%

Ta có:
\(d_{A/H2}=19,2\Rightarrow\overline{M_A}=19,2.2=38,4\left(\frac{g}{mol}\right)\)
\(\frac{n_{O2}}{n_{O3}}=\frac{48-38,4}{38,4-32}=\frac{3}{2}\)
Trong 1 mol hỗn hợp A có 0,6 mol O2 và 0,4 mol O3
\(2CO+O_2\rightarrow2CO_2\)
\(n_{CO}=0,6.2=1,2\left(mol\right)\)
PTHH:
\(2H_2+O_2\rightarrow2H_2O\)
\(d_{B/H2}=3,6\Rightarrow\overline{M_B}=3,6.2=7,2\left(\frac{g}{mol}\right)\)
\(\frac{n_{H2}}{n_{CO}}=\frac{7,2-2}{28-7,2}=\frac{1}{4}\)
Trong 1 mol B có 0,2 mol H2 và 0,8 mol CO
\(n_A=\frac{0,2}{2}+\frac{0,8}{2}=0,5\left(mol\right)\)

Phân tử khối trung bình của A = 19,2 x 2 = 38,4
Gọi a là tỷ lệ %số mol O2 trong A, ta có phương trình: 32a + 48(1 - a) = 38,4 --> a = 0,6
--> hỗn hợp A có 60% O2 và 40% O3
Phân tử khối trung bình của B = 3,6 x 2 = 7,2
Gọi b là tỷ lệ %số mol H2 trong B, ta có phương trình: 2b + 30(1 - b) = 7,2
--> b = 0,8142857
--> hỗn hợp B có 81,42857% H2 và 18,57143% CO Phương trình phản ứng:
H2 + [O] = H2O (1) CO + [O] = CO2 (2)
Từ phương trình phản ứng, ta thấy số mol nguyên tử [O] cần dùng để đốt cháy hoàn toàn hỗn hợp B bằng đúng số mol hỗn hợp B.
Trong 1 mol A, số mol nguyên tử [O] = 2 x 0,6 + 3 x 0,4 = 2,4 mol nguyên tử [O]. Vậy, số mol A cần dùng để đốt cháy hoàn toàn 1 mol B = 1/2,4 mol
=> Đáp án C

a) PTTH: \(2H_2+O_2\rightarrow2H_2O\)
\(C_2H_2+\dfrac{5}{2}O_2\underrightarrow{t^o}2CO_2+H_2O\)
b) Ta có: \(\left\{{}\begin{matrix}\overline{M}_{hhkhí}=0,5\cdot28=14\\n_{hhkhí}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\end{matrix}\right.\)
Theo phương pháp đường chéo, ta có: \(\dfrac{n_{H_2}}{n_{C_2H_2}}=\dfrac{12}{12}=1\)
\(\Rightarrow n_{H_2}=n_{C_2H_2}=0,3\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{H_2}=\dfrac{0,3}{0,6}\cdot100\%=50\%\\\%V_{C_2H_2}=50\%\\\%m_{H_2}=\dfrac{0,3\cdot2}{5,6}\cdot100\%\approx10,71\%\\\%m_{C_2H_4}=89,29\%\end{matrix}\right.\)

PTHH của các phản ứng :
2CO + O 2 → 2C O 2 (1)
3CO + O 3 → 3C O 2 (2)
Trong 1 mol hỗn hợp khí A có 0,6 mol O 3 và 0,4 mol O 2
Theo (1): 0,6 mol O 2 đốt cháy được 1,2 mol CO.
Theo (2) : 0,4 mol O 3 đốt cháy được 1,2 mol CO.
Kết luận : 1 mol hỗn hợp khí A đốt cháy được 2,4 mol khí CO.

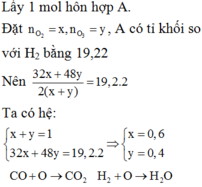
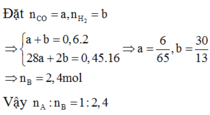
 Tham khảo cách làm nhé!
Tham khảo cách làm nhé!