Để xác định hàm lượng của bạc trong hợp kim, người ta hoà tan 0,5 gam hợp kim đó vào dung dịch axit nitric. Cho thêm dung dịch axit HCl dư vào dung dịch trên, thu được 0,398 gam kết tủa. Tính hàm lượng của bạc trong hợp kim.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(Đặt:m_{Ag}=a\left(a>0\right)\left(g\right)\\ 3Ag+4HNO_3\rightarrow3AgNO_3+NO+2H_2O\\ AgNO_3+HCl\rightarrow AgCl+HNO_3\\ n_{AgCl}=n_{AgNO_3}=n_{Ag}=\dfrac{a}{108}\left(mol\right)\\ m_{\downarrow}=\left(0,5-a\right)+\dfrac{a}{108}.143,5\\ \Leftrightarrow0,398=\left(0,5-a\right)+\dfrac{143,5}{108}a\\ \Leftrightarrow a=\left(âm\right)??\)

Ag → Ag+ + 1e
Ag+ + HCl → AgCl ↓ + H+
Số mol kết tủa là
nAgCl = 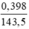 (mol)
(mol)
Theo pt nAg = nAg+ = nAgCl = 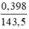 (mol)
(mol)
Khối lượng Ag là: mAg = 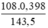 = 0,3 (g)
= 0,3 (g)
%mAg= 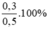 = 60%
= 60%

nH2 = 6,72/22,4 = 0,3 (mol)
PTHH: 2Al + 6HCl -> 2AlCl3 + 3H2
Mol: 0,2 <--- 0,6 <--- 0,2 <--- 0,3
mAl = 0,2 . 27 = 5,4 (g)
mAg = 16,2 - 5,4 = 10,8 (g)
mHCl (p/ư) = 0,6 . 36,5 = 21,9 (g)
mHCl (ban đầu) = 21,9/(100% - 20%) = 27,375 (g)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,9 0,3
\(m_{Al}=0,2\cdot27=5,4g\)\(\Rightarrow m_{Ag}=16,2-5,4=10,8g\)
a)\(\%m_{Al}=\dfrac{5,4}{16,2}\cdot100\%=33,33\%\)
\(\%m_{Mg}=100\%-33,33\%=66,67\%\)
b)\(\Sigma n_{HCl}=0,9mol\Rightarrow m_{HCl}=32,85g\)
Lượng axit đã lấy:
\(m_{ddHCl}=\dfrac{32,85}{20\%}\cdot100\%=164,25g\)


BTKL: mD + mNaHCO3 = mCO2 + mE
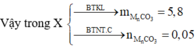
mD + 179,88 = 44.0,2 + 492 => mD = 320,92
BTKL: mMg + mddHCl = mH2 + mD
=> 24 . 0,4 + mddHCl = 2 . 0,4 + 320,92 => mddHCl = 312,12
=> C%HCl = 11,69%
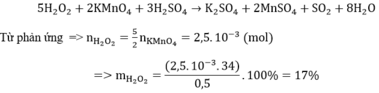

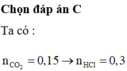

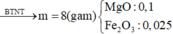


Ag + 2 HNO3 → AgNO3 + NO2 + H2O (1)
AgNO3 + HCl → AgCl + HNO3 (2)
Từ (1) và (2), ta có: nAg =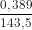 = 0,00277 (mol)
= 0,00277 (mol)
=> %mAg= .100% = 59,9%
.100% = 59,9%