1. cho 3,36l oxi phản ứng hoàn toàn với 1 kim loại hóa trị III thu được 10,2g oxit. Tên kim loại?
2. đốt cháy 18g kim loại hóa trị II cần dùng vừa đủ 8,4l O2 (đktc). tên kim loại?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

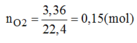
Gọi A là kí hiệu của kim loại có hóa trị III, M A là nguyên tử khối của A.
Ta có PTHH:

Theo PTHH trên ta có:
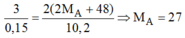
Vậy A là nhôm.

ta có Ax + By = 23.8 (1) ( dữ kiện : khối lượng hỗn hợp kim loại )
x+ 3y = 0.8 ( dữ kiện : cần 8.96 lít O2 )
và có dữ kiện cuối cùng là hỗn hợp chất rắn sau khi bị khử bởi H2 còn lại 33.4 gam
thì ta tính đọc số mol Oxi còn trong hỗn hợp là 0.6
TH1 chỉ có A bị khử thì số mol oxi trong hỗn hợp trên là của B  3y = 0.6
3y = 0.6  x = 0.2
x = 0.2
mà B hóa trị 3 và không bị khủ thì chỉ có thể là Al  A là Zn
A là Zn
TH2 chỉ có B bị khử ta tính được số mol trong hỗn hợp trên là của A  x =0.6 y = 0.2/3
x =0.6 y = 0.2/3
ta tính : ráp số vào phương trình (1) ta được 0.6A +0.4/3B =23.8
từ đó ta có 23.8 / 0.6 < A,B< 23.8*3/0.4
lúc này ta lục bảng tuần hoàn và thế vô đều không thỏa mãn nên th2 loại
vậy kim loại cần tìm là Zn và Al

ta có Ax + 2By = 23.8 (1) ( dữ kiện : khối lượng hỗn hợp kim loại )
x+ 3y = 0.8 ( dữ kiện : cần 8.96 lít O2 )
và có dữ kiện cuối cùng là hỗn hợp chất rắn sau khi bị khử bởi H2 còn lại 33.4 gam
thì ta tính đọc số mol Oxi còn trong hỗn hợp là 0.6
TH1 chỉ có A bị khử thì số mol oxi trong hỗn hợp trên là của B  3y = 0.6
3y = 0.6  x = 0.2
x = 0.2
mà B hóa trị 3 và không bị khủ thì chỉ có thể là Al  A là Zn
A là Zn
TH2 chỉ có B bị khử ta tính được số mol trong hỗn hợp trên là của A  x =0.6 y = 0.2/3
x =0.6 y = 0.2/3
ta tính : ráp số vào phương trình (1) ta được 0.6A +0.4/3B =23.8
từ đó ta có 23.8 / 0.6 < A,B< 23.8*3/0.4
lúc này ta lục bảng tuần hoàn và thế vô đều không thỏa mãn nên th2 loại
vậy kim loại cần tìm là Zn và Al

Cách khác:
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\Rightarrow m_{O_2}=0,15.32=4,8\left(g\right)\\ Đặt.KL:B\\ 4B+3O_2\rightarrow\left(t^o\right)2B_2O_3\\ ĐLBTKL:m_B+m_{O_2}=m_{oxit}\\ \Leftrightarrow m_B+4,8=10,2\\ \Leftrightarrow m_B=5,4\left(g\right)\\ Mà:n_B=\dfrac{4}{3}.n_{O_2}=0,2\left(mol\right)\\ \Rightarrow M_B=\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow B\left(III\right):Nhôm\left(Al=27\right)\)

PTHH : 4R + 3O2 ---> 2R2O3
nO2 = 0,15 ( mol )
nR = 4/3 . nO2 = 0,2 ( mol )
nR2O3 = 0,1 ( mol )
=> M = 10,2 : 0,1 = 102 ( đvC )
Ta có:
R.2 + 16.3 = 102
-> R = 27 ( Al )
\(n_{O2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(4R+3O_2\underrightarrow{t^o}2R_2O_3|\)
4 3 2
0,2 0,15
Theo định luật bảo toàn khối lượng :
\(m_R+m_{O2}=m_{R2O3}\)
\(m_R+\left(0,15.32\right)=10,2\)
⇒ \(m_R=10,2-4,8=5,4\left(g\right)\)
\(n_R=\dfrac{0,15.4}{3}=0,2\left(mol\right)\)
⇒ \(M_R=\dfrac{5,4}{0,2}=27\) (g/mol)
Vậy kim loại R là nhôm
Chúc bạn học tốt

Bài 1:
Gọi KL cần tìm là A.
PT: \(A+2HCl\rightarrow ACl_2+H_2\)
Ta có: \(n_{HCl}=0,1.6=0,6\left(mol\right)\)
Theo PT: \(n_A=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{7,2}{0,3}=24\left(g/mol\right)\)
Vậy: KL cần tìm là Mg.
Bài 2:
PT: \(2R+6HCl\rightarrow2RCl_3+3H_2\)
Ta có: \(n_{H_2}=\dfrac{9,408}{22,4}=0,42\left(mol\right)\)
Theo PT: \(n_R=\dfrac{2}{3}n_{H_2}=0,28\left(mol\right)\)
\(\Rightarrow M_R=\dfrac{7,56}{0,28}=27\left(g/mol\right)\)
Vậy: R là Al.

4Al+3O2-to>2Al2O3
0,04---0,03------0,02 mol
n Al=\(\dfrac{1,08}{27}\)=0,04 mol
=>VO2=0,03.22,4=0,672l
b)
2A+O2-to>2AO
0,06--0,03 mol
=>\(\dfrac{3,84}{A}=0,06\)
=>A=64 :=>Al là Đồng
Bài 1 :
Gọi nguyên tố cần tìm là X
Ta có CTHH : X2O3
noxi = \(\frac{V}{22,4}\)= \(\frac{3,36}{22,4}\)= 0,15 (mol)
PTHH : 4X + 3O2 -> 2X2O3
4mol 3mol 2mol
0,2 0,15 0,1
\(M^{_{X_2O_3}}\)= \(\frac{m}{n}\)= \(\frac{10,2}{0,1}\)= 102 (g/mol)
=> 2.X + 3.O2 = 102 \(n_{O_2}\)
2.X + 3.16 = 102
2.X = 102 - 48 = 54
X = 54 : = 27 (g/mol)
Vậy X là Al ( nhôm)
Bài 2 :
Gọi nguyên tố cần tìm là R
Ta có CTHH : RO
\(n_{O_2}\)= \(\frac{V}{22,4}\)= \(\frac{8,4}{22,4}\)= 0,375 (mol)
PTHH: 2R + O2 -> 2RO
2mol 1mol 2mol
0,75 0,375 0,75
MR = \(\frac{m}{n}\)= \(\frac{18}{0.75}\)= 24 (g/mol)
Vậy R là Mg ( Magie)
Bài 2:
Gọi CTHH của kim loại có hóa trị II cần tìm là X.
PTHH: 2X + O2 -> 2XO
Ta có:
\(n_{O_2}=\frac{8,4}{22,4}=0,375\left(mol\right)\)
Theo PTHH và đề bài, ta có:
\(n_R=2.n_{O_2}=2.0,375=0,75\left(mol\right)\)
=> \(M_R=\frac{18}{0,75}=24\left(\frac{g}{mol}\right)\)
Vậy: Kim loại R có hóa trị II cần tìm là Mg (magie).