1/Cần bao nhiêu gam Oxi để đốt cháy hoàn toàn:
+ 5mol Cacbon
+ 5mol Lưu huỳnh
2/ Trong giờ thực hành thí nghiệm, một HS đốt cháy 3,2g lưu huỳnh trong 1,12 lít Oxi (đktc). Vậy theo em lưu huỳnh cháy hết hay còn dư.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

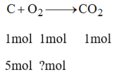
Số mol O 2 :
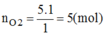
Khối lượng O 2 :
m O 2 = n O 2 . M O 2 = 5.32 = 160(g)
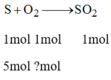
Số mol O 2 :
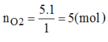
Khối lượng O 2 :
m O 2 = n O 2 . M O 2 = 5.32 = 160(g)

a, PTHH: C + O2 ➝ CO2
Theo pt: 1 1 1 (mol)
Theo bài ra: 5 → 5 (mol)
⇒mO2= 5x32= 160(g)
PTHH: S + O2 ➞ SO2
Theo pt: 1 1 1 (mol)
Theo bài ra: 5 → 5 (mol)
⇔mO2= 5x32=160(g)
b, nO2= 1,12/22,4=0,05(mol)→mO2=1,6(g)
PTHH: S + O2 ➝ SO2
Theo pt: 32 32 64 (g)
Theo bài ra: 3,2 1,6 (g)
Phản ứng: dư hết
⇒mS dư = 3,2 - 1,6=1,6(g)
Vậy lưu huỳnh dư và dư 1,6g
TICK CHO MIK NHOA!!!
a, \(C+O_2\underrightarrow{^{to}}CO_2\)
\(n_{O2}=5\left(mol\right)\rightarrow m_2=160\left(g\right)\)
\(S+O_2\underrightarrow{^{to}}SO_2\)
\(n_{O2}=5\left(mol\right)\rightarrow m_{O2}=160\left(g\right)\)
b, \(n_S=0,1\left(mol\right);n_{O2}=0,05\left(mol\right)\)
Nên S dư 0,05 (mol) \(\rightarrow m_{S_{du}}=1,6\left(g\right)\)

\(a,PTHH:S+O_2\underrightarrow{t^o}SO_2\left(1\right)\)
\(n_S=\dfrac{m}{M}=\dfrac{9,6}{32}=0,3\left(mol\right)\)
\(Theo.PTHH\left(1\right):n_O=n_S=0,3\left(mol\right)\)
\(PTHH:2KClO_3\underrightarrow{t^o}2KCl+3O_2\\ Theo.PTHH\left(2\right):n_{KClO_3}=\dfrac{2}{3}.n_{O_2}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ m_{KClO_3}=n.M=0,2.122,5=24,5\left(g\right)\)
\(b,V_{O_2\left(đktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\\ \Rightarrow V_{kk\left(đktc\right)}=5.V_{O_2}=5.4,48=22,4\left(l\right)\)

nS=mS/MS=3,2/32=0,1(mol)
nO2=VO2/22,4=32/22,4=1,42(mol)
PTHH: S + O2 --> SO2 (1)
BĐ: 0,1 1,42
PỨ: 0,1-->0,1-->0,1
SPỨ: 0--->1,32-->0,1
a) Từ PT(1)=>O2 dư
VO2(dư)=nO2(dư) .22,4=1,32 .22,4=29,568(l)
b) Từ PT(1)=>nSO2=0,1(mol)
=>mSO2=n.M=0,1 .64=6,4(g)
Mình sửa lại nha mình nhầm ạ

Gọi nC = a (mol); nS = b (mol)
12a + 32b = 12 (1)
PTHH:
C + O2 -> (t°) CO2
a ---> a ---> a
S + O2 -> (t°) SO2
b ---> b ---> b
44a + 64b = 28 (2)
Từ (1)(2) => a = 0,2 (mol); b = 0,3 (mol)
nO2 = 0,2 + 0,3 = 0,5 (mol)
VO2 = 0,5 . 22,4 = 11,2 (l)
Bài 1:
a) PTHH: C+ O2 -to-> CO2
Theo PTHH và đề bài, ta có:
\(n_{O_2}=n_C=5\left(mol\right)\)
Khối lượng khí O2 cần dùng cho phản ứng:
\(m_{O_2}=n_{O_2}.M_{O_2}=5.32=160\left(g\right)\)
Bài 1 mình không hiểu lắm.
Mình làm bài 2 nha.
Bài 2:
Ta có:
\(n_S=\frac{m_S}{M_S}=\frac{3,2}{32}=0,1\left(mol\right)\)
\(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: S + O2 -to-> SO2
Theo PTHH và đề bài ta có:
\(\frac{n_{S\left(đềbài\right)}}{n_{S\left(PTHH\right)}}=\frac{0,1}{1}=0,1>\frac{n_{O_2\left(đềbài\right)}}{n_{O_2\left(PTHH\right)}}=\frac{0,05}{1}=0,05\)
Vậy: O2 phản ứng hết còn S dư .