cho dòng khí co dư qua hỗn hợp 2 oxit cuo và fe3o4 nung nóng thu được 29,6 hỗn hợp 2 kim loại trong đó sắt nhiều hơn đồng là 4g. tính thể tích khí co cần dùng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PTHH của các phản ứng:
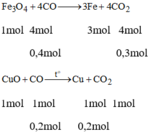
Gọi x là khối lượng của Cu sau phản ứng
→ Khối lượng của sắt sau phản ứng là x+4
Theo đề bài ta có: x + x + 4 = 29,6 → x = 12,8(g)
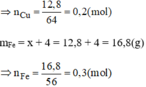
Theo pt: 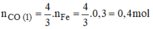
n C O ( 2 ) = n C u = 0 , 2 m o l
n C O = (0,4 + 0,2).22,4 = 13,44(l)

\(CO\left(x\right)+CuO\left(x\right)\rightarrow Cu\left(x\right)+CO_2\)
\(3CO\left(3y\right)+Fe_2O_3\left(y\right)\rightarrow3CO_2+2Fe\left(2y\right)\)
Gọi số mol của CuO và Fe2O3 lần lược là x, y thì ta có:
\(\left\{\begin{matrix}64x+56y=29,6\\56y-64x=4\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}x=0,2\\y=0,3\end{matrix}\right.\)
\(\Rightarrow n_{CO}=0,2+3.0,3=1,1\)
\(\Rightarrow V_{CO}=1,1.22,4=24,64\)

a)
Ca(OH)2 + CO2 --> CaCO3 + H2O
CO + CuO --to--> Cu + CO2
b)
\(n_{CaCO_3}=\dfrac{1}{100}=0,01\left(mol\right)\)
PTHH: Ca(OH)2 + CO2 --> CaCO3 + H2O
0,01<-----0,01
\(n_{CuO}=\dfrac{0,64}{64}=0,01\left(mol\right)\)
PTHH: CO + CuO --to--> Cu + CO2
0,01<--------------0,01
=> Vhh khí = (0,01 + 0,01).22,4 = 0,448 (l)
VCO = 0,01.22,4 = 0,224 (l)
VCO2 = 0,01.22,4 = 0,224 (l)

\(m_{Cu}=\dfrac{29,6-4}{2}=12,8(g)\\ \Rightarrow m_{Fe}=12,8+4=16,8(g)\\ PTHH:CuO+H_2\xrightarrow{t^o}Cu+H_2O\\ Fe_3O_4+4H_2\xrightarrow{t^o}3Fe+4H_2O\\ \Rightarrow \Sigma n_{H_2}=n_{Cu}+3n_{Fe}=\dfrac{12,8}{64}+\dfrac{3}{4}.\dfrac{16,8}{56}=0,6(mol)\\ \Rightarrow V_{H_2}=0,6.22,4=13,44(l)\)

Ta có: \(\left\{{}\begin{matrix}m_{Fe}=\dfrac{59,2+8}{2}=33,6\left(g\right)\\m_{Cu}=59,2-33,6=25,6\left(g\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}n_{Fe}=\dfrac{33,6}{56}=0,6\left(mol\right)\\n_{Cu}=\dfrac{25,6}{64}=0,4\left(mol\right)\end{matrix}\right.\)
PTHH:
\(Fe_3O_4+4H_2\xrightarrow[]{t^o}3Fe+4H_2O\)
0,8<----0,3
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
0,4<---0,4
`=> V_{H_2} = (0,4 + 0,8).22,4 = 26,88 (l)`
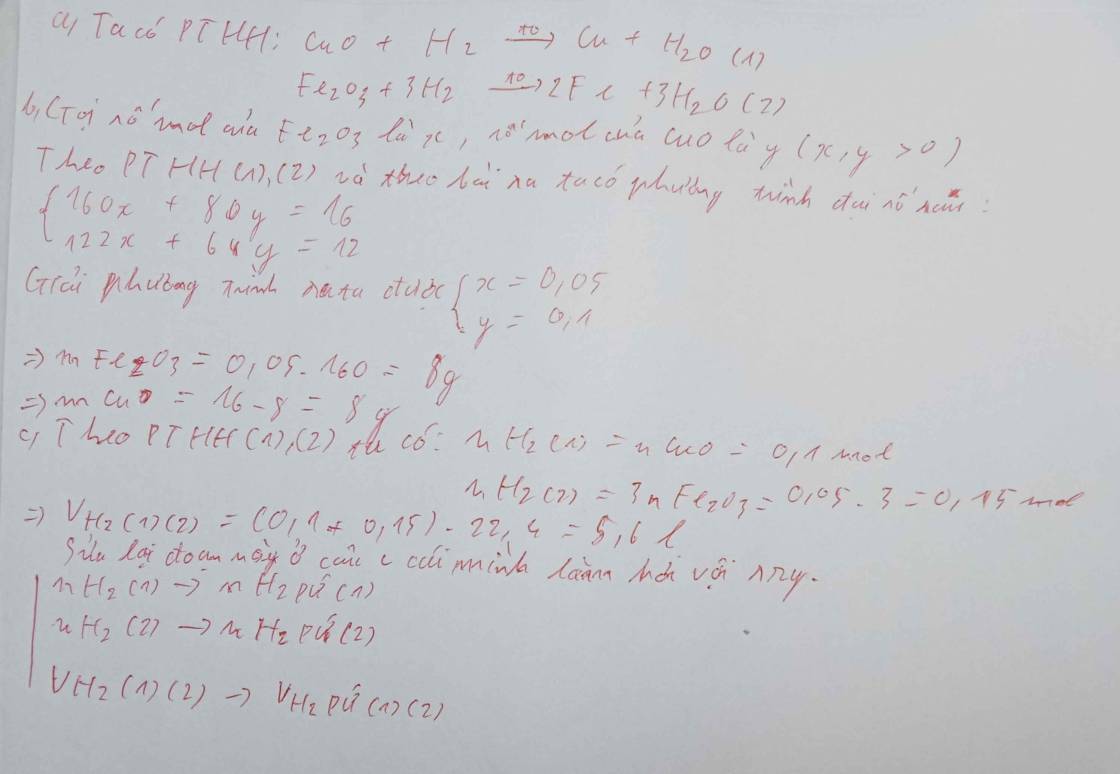
Ta có: \(m_{Fe}\) + \(m_{Cu}\) = 29,6
hay\(m_{Cu}\) +4 + \(m_{Cu}\) = 29,6
2\(m_{Cu}\) = 25,6
\(m_{Cu}\) =12,8(g)
=> \(m_{Fe}\) = 16,8(g)
Số mol của 12,8 g Cu:
\(\frac{12,8}{64}\)= 0,2(mol)
Số mol của 16,8g Fe:
\(\frac{16,8}{56}\)=0,3(mol)
CO + CuO \(\rightarrow\) Cu + C\(O_2\)
1(mol) 1(mol)
0,2(mol) 0,2(mol)
4CO + \(Fe_3\)\(O_4\) \(\rightarrow\) 3Fe + 4C \(O_2\)
4(mol) 3(mol)
0,4(mol) 0,3(mol)
Thể tích CO cần dùng:
(0,2+0,4).22,4= 13,44(l)
PTHH: Fe3O4+4Co->3Fe+4Co2 (1)
CuO+Co->Cu+Co2 (2)
Lại có: mFe+mCu=29,6
mFe-mCu=4
=>mFe=16,8=> nFe=0.3mol
mCu=12,8g=>nCu=0.2mol
Theo PTHH(1)
nFe:nCo= 3:4=> nCo=0,3.4/3=0,4mol
nCu:nCo= 1:1 => nCo= 0,2mol
=> nCo=0,6mol=13,44(l)