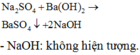trình bày phương pháp hóa học để phân biệt các dung dịch : NH3 , Na2SO4 , NH4Cl , (NH4)2SO4. Viết các phương trình hóa học đã dùng .
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Trích mẫu thử
Cho dung dịch $Ba(OH)_2$ vào :
- mẫu thử tạo khí mùi khai là $NH_4Cl$
$2NH_4Cl + Ba(OH)_2 \to 2NH_3 + BaCl_2 + 2H_2O$
- mẫu thử tạo khí mùi khai và kết tủa trắng là $(NH_4)_2SO_4$
$(NH_4)_2SO_4 + Ba(OH)_2 \to BaSO_4 + 2NH_3 + 2H_2O$
- mẫu thử tạo kết tủa trắng là $Na_2SO_4$
$Ba(OH)_2 + Na_2SO_4 \to BaSO_4 + 2NaOH$
- mẫu thử không hiện tượng là $NH_3$

Cho quỳ tím vào từng ống: ống màu xanh là dung dịch NH3; hai ống có màu hồng là NH4Cl và (NH4)2SO4; ống không có hiện tượng gì là Na2SO4.
Cho Ba(OH)2 vào hai ống làm hồng quỳ tím. Nếu thấy ống nào có khí bay ra mùi khai là NH4Cl, ống vừa có khí bay ra mùi khai vừa có kết tủa là (NH4)2SO4.
(NH4)2SO4 + Ba(OH)2 → BaSO4 ↓ + 2NH3 ↑ + 2H2O
2NH4Cl + Ba(OH)2 → BaCl2 + 2NH3 + 2H2O

- Dùng quỳ tím
+) Hóa đỏ: HCl và AgNO3 (Nhóm 1)
+) Hóa xanh: K3PO4
+) Không đổi màu: NaNO3 và (NH4)2CO3
- Đổ dd BaCl2 vào từng nhóm
+) Xuất hiện kết tủa: AgNO3 (Nhóm 1) và (NH4)2CO3 (Nhóm 2)
PT: \(Ag^++Cl^-\rightarrow AgCl\downarrow\)
\(Ba^{2+}+CO_3^{2-}\rightarrow BaCO_3\downarrow\)
+) Không hiện tượng: HCl (Nhóm 1) và NaNO3 (Nhóm 2)

Phương pháp: thử 5 hóa chất hữu dụng: Ba(OH)2, H2SO4, AgNO3, Quì, HCl
|
|
NH4Cl |
(NH4)2SO4 |
NaNO3 |
| Ba(OH)2 |
↑NH3 Mùi khai |
↑NH3 Mùi khai BaSO4 ↓trắng |
x |
|
|
MgCl2 |
FeCl2 |
FeCl3 |
|
|
Mg(OH)2 Trắng |
Fe(OH)2 xanh |
Fe(OH)3 Nâu đỏ |
|
|
Al(NO3)3 |
|
|
|
|
Al(OH)3 Trắng sau đó tan dần |
|
|

- Cho NaOH tác dụng với các dung dịch:
+ Không hiện tượng: NaCl, BaCl2 (1)
+ Có khí mùi khai thoát ra: NH4Cl
\(NH_4Cl+NaOH->NaCl+NH_3+H_2O\)
+ Xuất hiện kết tủa trắng xanh, hóa nâu sau 1 thời gian: FeCl2
\(FeCl_2+2NaOH->Fe\left(OH\right)_2\downarrow+2NaCl\)
\(4Fe\left(OH\right)_2+O_2+2H_2O->4Fe\left(OH\right)_3\downarrow\)
+ Xuất hiện kết tủa trắng: Ba(HCO3)2, MgCl2 (2)
\(Ba\left(HCO_3\right)_2+2NaOH->Na_2CO_3+BaCO_3\downarrow+2H_2O\) (*)
\(MgCl_2+2NaOH->Mg\left(OH\right)_2\downarrow+2NaCl\)
- Đun nóng dung dịch ở (2)
+ Sủi bọt khí, xuất hiện kết tủa trắng:
\(Ba\left(HCO_3\right)_2\underrightarrow{t^o}BaCO_3\downarrow+CO_2\uparrow+H_2O\)
+ Không hiện tượng: MgCl2
- Lọc kết tủa của dung dịch thu được từ (*), ta thu được dung dịch Na2CO3. Cho dd Na2CO3 tác dụng với dung dịch ở (1)
+ Không hiện tượng: NaCl
+ Xuất hiện kết tủa trắng: BaCl2
\(BaCl_2+Na_2CO_3->BaCO_3\downarrow+2NaCl\)

Để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4, có thể dùng thuốc thử lần lượt là: dd BaCl2, dd NaOH.

trước tiên cho quỳ tím ẩm, lọ nào đổi màu ->màu xanh thì là nh3
3 lọ mất nhãn còn lại cho ba(oh)2 vào, đun nhẹ
+lọ chỉ có kết tủa trắng là na2so4
+lọ có sủi bọt khí (nh3) là nh4cl
+lọ vừa có kết tủa trắng vừa có sủi bọt khí (nh3) là (nh4)2so4
phương trình:
Na2so4+ba(oh)2 -> baso4 (kết tủa trắng) + 2naoh
2nh4cl + ba(oh)2 -> bacl2 + 2nh3(bay hơi, mùi khai ) + 2h2o
(nh4)2so4 + ba(oh)2 -> baso4 (kt) + 2nh3(bay hơi) + 2h2o