Hỗn hợp X nặng m gam, gồm : Fe, FeO, Fe2O3 và CuO. Người ta cho hỗn hợp khí Y gồm CO2 và CO đi qua ống sứ chứa m gam X và nung nóng ở nhiệt độ cao, thu được 20 gam chất rắn A và khí Z. Dẫn toàn bộ khí Z đi qua dung dịch nước vôi trong dư, thu được 40 gam kết tủa và còn lại một khí G thoát ra có thể tích bẳng 20% thể tích khí Z nói trên. Cho biết khí Y có khối lượng riêng bằng 1,393 g/lít (đktc)
a) Viết các PTHH xảy ra
b) Tính m? Biết hiệu suất các phản ứng đều là 100%
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{\text{kết tủa}}=m_{CaCO_3}=7\left(g\right)\\ \rightarrow n_{CaCO_3}=\dfrac{7}{100}=0,07\left(mol\right)\)
PTHH:
\(CO_2+Ca\left(OH\right)_2\rightarrow CaCO_3\downarrow+H_2O\)
0,07<--------------------0,07
\(O+CO\xrightarrow[]{t^o}CO_2\)
0,07<--------0,07
\(\rightarrow m_O=0,07.16=1,12\left(g\right)\)
Áp dụng ĐLBTNT:
\(m=m_X=m_Y+m_O=2,8+1,12=3,92\left(g\right)\)

\(m_{H_2SO_4}=\dfrac{100.96,48}{100}=96,48\left(g\right)\)
\(m_{dd.sau.thí.nghiệm}=\dfrac{96,48.100}{90}=107,2\left(g\right)\)
=> \(m_{H_2O\left(thêm\right)}=107,2-100=7,2\left(g\right)\Rightarrow n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> nO(mất đi) = 0,4 (mol)
Có: mX = mY + mO(mất đi) = 113,6 + 0,4.16 = 120 (g)


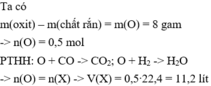
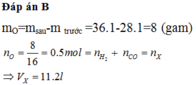

A, Gọi X,y lần lượt là số mol của Mg và Al
Pthh:
Mg + H2SO4---> MgSO4 + H2
X. X. X. X
2Al + 3H2SO4---> Al2(SO4)3+3H2
Y. 1.5y. Y. 1.5y
Ta có pt:
24x + 27y= 1.95
X+1.5y=2.24/22.4=0.1
=> X=0.025, Y=0.05
%Mg= 0.025×24×100)/1.95=30.8%
%Al= 100%-30.8%=69.2%
mH2SO4= 0.025+1.5×0.05=0.1g
mH2= (0.025+0.05)×2=0.15g
C, Mdd H2SO4 = 0.1/6.5×100=1.54g
MddY= 1.54+1.95-0.15=3.34g
%MgSO4 vs %Al2(SO4)3 b tự tính nha