Câu 1 Hợp chất oxit B có khối lượng mol phân tử là 142g/mol thành phần % các nguyên tố theo khối lượng là 43,66% P còn lại là oxi Xác định CTPT Câu 2 Tìm công thức hóa học của khí A biết a Khí A nặng hơn khí hidro là 22 lần b thành phần theo khối lượng khí A là 27,3% C còn lại là O câu 3 Hòa tan hoàn toàn 4g oxit(A là kim loại hóa trị II) cần 146g dung dịch HCl 10% Xác định công thức hóa học của oxit
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1 :
\(CT:P_xO_y\)
Ta có :
\(\dfrac{m_P}{m_O}=\dfrac{31}{24}\Rightarrow\dfrac{31x}{16y}=\dfrac{31}{24}\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
\(CT:P_2O_3\)

Bài 2:
\(Đặt.CTTQ.của.A:H_xS_yO_z\left(x,y,z:nguyên,dương\right)\\ Ta.có:\left\{{}\begin{matrix}x=\dfrac{98.2,04\%}{1}=2\\y=\dfrac{98.32,65\%}{32}=1\\z=\dfrac{98.\left(100\%-2,04\%-32,65\%\right)}{16}=4\end{matrix}\right.\\ \Rightarrow x=2;y=1;z=4\\ \Rightarrow CTHH:H_2SO_4\)
Bài 1: Sửa đề 59,2% Al thành 52,9% Al
\(Đặt.CTTQ:Al_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{52,9\%.102}{27}\approx2\\ \Rightarrow y\approx\dfrac{\left(100\%-52,9\%\right).102}{16}\approx3\\ \Rightarrow CTHH:Al_2O_3\)

Trong 1 mol hợp chất:
$n_H=\dfrac{98.2,04\%}{1}\approx 2(mol)$
$n_S=\dfrac{98.32,65\%}{32}\approx 1(mol)$
$n_O=\dfrac{98-2-32}{16}=4(mol)$
$\to CTHH:H_2SO_4$

Câu1) nCO2 =m/M=11/44=0,25(mol)
nH2= 9.1023/6.1023=1,5(mol)
VH2 =n.22,4=1,5.22,4=33,6(l)

\(m_{Fe}=180.31,11\%=56\left(g\right)\\ m_N=180.15,56\%=28\left(g\right)\\ m_O=180-56-28=96\left(g\right)\)
\(n_{Fe}=\dfrac{56}{56}=1\left(mol\right)\\ n_N=\dfrac{28}{14}=2\left(mol\right)\\ n_O=\dfrac{96}{16}=6\left(mol\right)\)
\(CTHH:Fe\left(NO_3\right)_2\)
(đề lỗi nên mik sửa Bari thành Sắt nhé chứ Bari nặng tới 137 g/mol)

\(m_{Fe}=\%Fe.M_X=28\%.400=112\left(g\right)\\ m_S=\%S.M_X=24\%.400=96\left(g\right)\\ m_O=m_X-m_{Fe}-m_S=400-112-96=192\left(g\right)\)
\(\Rightarrow n_{Fe}=\dfrac{m}{M}=\dfrac{112}{56}=2\left(mol\right)\)
\(m_S=\dfrac{m}{M}=\dfrac{96}{32}=3\left(mol\right)\)
\(m_O=\dfrac{m}{M}=\dfrac{192}{16}=12\left(mol\right)\)
\(CTHH:Fe_2\left(SO_4\right)_3\)
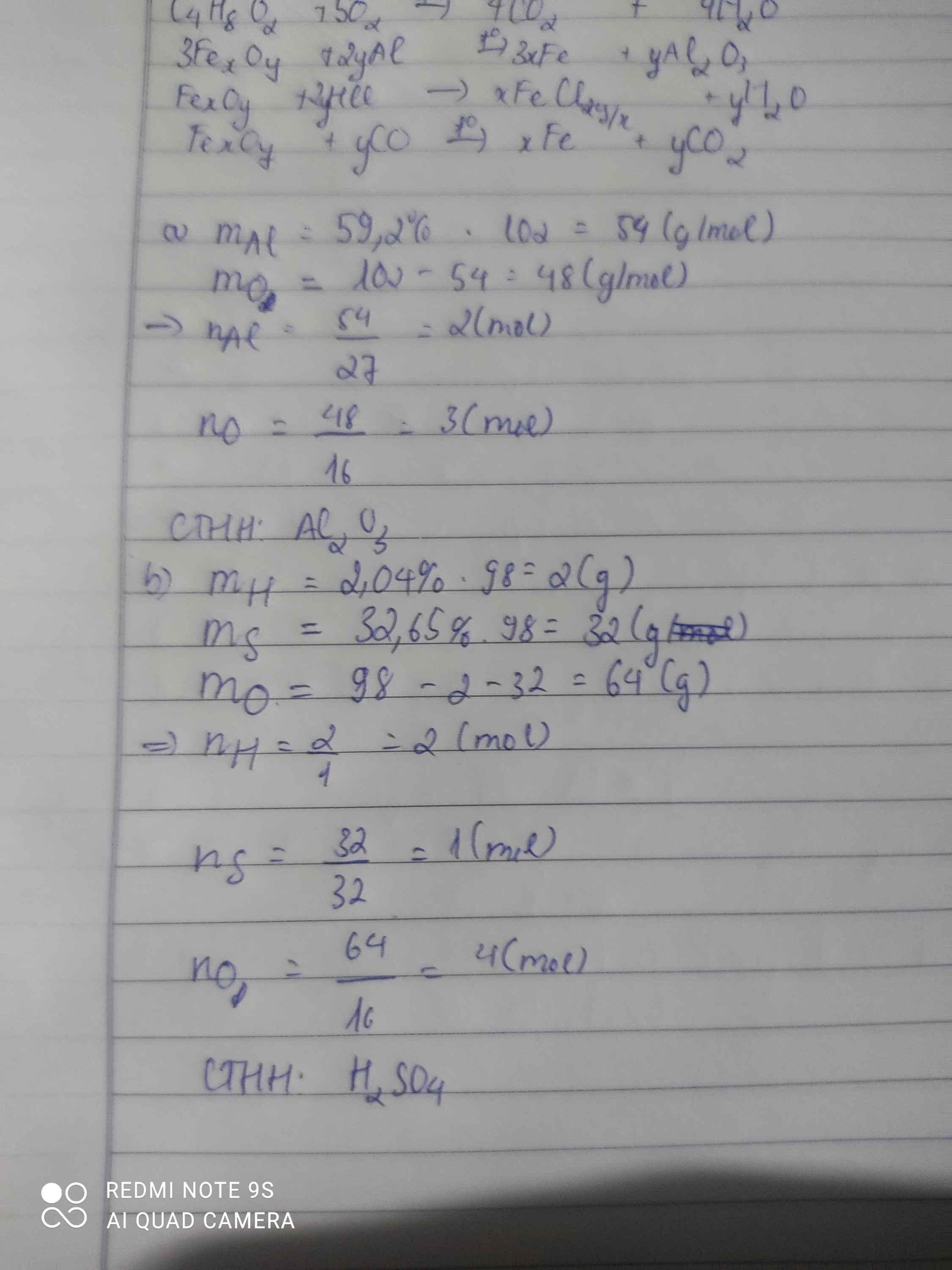

Câu 1 :
\(CT:P_xO_y\)
\(\%P=\dfrac{31x}{142}\cdot100\%=43.66\%\)
\(\Rightarrow x=2\)
\(M_B=31\cdot2+16\cdot y=142\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow y=5\)
\(CTPT:P_2O_5\)
Câu 2 :
\(a.\)
\(M_A=22\cdot2=44\left(\dfrac{g}{mol}\right)\)
\(CT:C_xO_y\)
\(\%C=\dfrac{12x}{44}\cdot100\%=27.3\%\)
\(\Rightarrow x=1\)
\(M_A=12+32\cdot y=44\left(\dfrac{g}{mol}\right)\)
\(\Rightarrow y=2\)
\(CT:CO_2\)