Đốt cháy 11,2 gam Fe ngoài không khí một thời gian thu được 15,04 gam hỗn hợp X gồm Fe FeO Fe304 Fe2O3 cho toàn bộ X tác dụng với H2SO4 đặc nóng thu được V lít (điều kiện tiêu chuẩn )khí SO2 (sản phẩm khử duy nhất) .Tính V
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Đáp án A
Ta có, nFe = 0,225 mol và nSO2 = 0,1875 mol
Quy hỗn hỗn hợp X về 2 nguyên tố Fe và O
Quá trình nhường: Fe0 → Fe+3 + 3e
Quá trình nhận e: O0 + 2e → O-2
S+6 + 2e → S+4
Áp dụng định luật bảo toàn electron ta có:
0,675 = 2x + 0,375 → x = 0,15
Mặt khác ta có: nên: m = 12,6 + 0,15.16 = 15 (gam).

Ta có: \(n_{Fe}=\dfrac{12,6}{56}=0,225\left(mol\right)\)
Coi X gồm Fe và O.
BTNT Fe: nFe (X) = 0,225 (mol)
Ta có: \(n_{SO_2}=\dfrac{1,68}{22,4}=0,075\left(mol\right)\)
BT e, có: 3nFe = 2nO + 2nSO2 ⇒ nO = 0,2625 (mol)
⇒ m = mFe + mO = 0,225.56 + 0,2625.16 = 16,8 (g)

Đáp án B
Xét giai đoạn A tác dụng với H2SO4 đặc, nóng, dư:
Số mol SO2 thu được là: n SO 2 = 0 , 15 mol
Qui đổi hỗn hợp A thành Fe : a mol; O : b mol
![]()
Sơ đồ phản ứng :
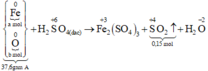
Các quá trình nhường, nhận electron:
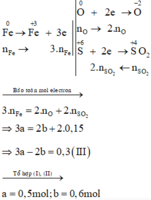
Xét giai đoạn để m gam Fe ngoài không khí:
Sơ đồ phản ứng :

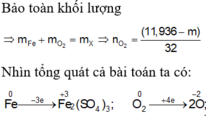
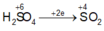
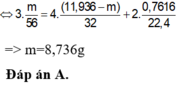



\(m_{O_2}=15.04-11.2=3.85\left(g\right)\)
\(n_{O_2}=\dfrac{3.85}{32}=0.1203125\left(mol\right)\)
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
Bảo toàn e :
\(n_{SO_2}=\dfrac{3\cdot0.2-0.1203125\cdot4}{2}=0.059375\left(mol\right)\)
\(V_{SO_2}=1.33\left(l\right)\)
lớp 9 đã học bảo toàn e rồi ợ ;-;