Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_{SO_4}=m_{muối.sunfat}-m_{kim.loai}=79,44-19,92=59,52\left(g\right)\)
=> \(n_{SO_4}=\dfrac{59,52}{96}=0,62\left(mol\right)\)
=> \(n_{H_2SO_4\left(pư\right)}=0,62\left(mol\right)\)
\(n_{O_2\left(pư\right)}=\dfrac{25,04-19,92}{32}=0,16\left(mol\right)\)
Bảo toàn O: \(n_{H_2O}=0,32\left(mol\right)\)
Bảo toàn H: \(n_{H_2}=\dfrac{0,62.2-0,32.2}{2}=0,3\left(mol\right)\)
=> V = 0,3.22,4 = 6,72 (l)

\(n_S = \dfrac{0,64}{32} = 0,02(mol)\)
Gọi \(n_{Cu} = a ; n_{Zn} = b\)
\(\Rightarrow 64a + 65b = 12,9(1)\)
Bảo toàn electron :
\(2n_{Cu} + 2n_{Zn} = 2n_{SO_2} + 6n_S\\ \Rightarrow 2a + 2b = 0,14.2 + 0,02.6(2)\)
Từ (1)(2) suy ra a = 0,1 ; b = 0,1
Vậy : \(\%m_{Cu} = \dfrac{0,1.64}{12,9}.100\% = 49,61\%\)

a) \(n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
0,05<-----------0,05---->0,075
=> \(\%Al=\dfrac{0,05.27}{14,15}.100\%=9,54\%\)
=> \(\%Cu=\dfrac{14,15-0,05.27}{14,15}.100\%=90,46\%\)
b) \(V_{H_2}=0,075.22,4=1,68\left(l\right)\)
c) \(n_{Cu}=\dfrac{14,15-0,05.27}{64}=0,2\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
0,05->0,0375
2Cu + O2 --to--> 2CuO
0,2-->0,1
=> \(V_{O_2}=\left(0,1+0,0375\right).22,4=3,08\left(l\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ m_{AlCl_3}=6,675\left(mol\right)\\ n_{AlCl_3}=\dfrac{6,675}{133,5}=0,05\left(mol\right)\\ \Rightarrow n_{Al}=n_{AlCl_3}=0,05\left(mol\right)\\ \Rightarrow m_A=0,05.27=1,35\left(g\right);m_{Cu}=14,15-1,35=12,8\left(g\right)\\ \%m_{Cu}=\dfrac{12,8}{14,15}.100\approx90,459\%\\ \Rightarrow\%m_{Al}\approx9,541\%\\ b,n_{Cu}=\dfrac{12,8}{64}=0,2\left(mol\right)\\ n_{H_2}=\dfrac{3}{2}.n_{Al}=\dfrac{3}{2}.0,05=0,075\left(mol\right)\\ \Rightarrow V=V_{H_2\left(đktc\right)}=0,075.22,4=1,68\left(l\right)\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Cu+O_2\rightarrow\left(t^o\right)2CuO\\ n_{O_2}=\dfrac{3}{4}.n_{Al}+\dfrac{1}{2}.n_{Cu}=\dfrac{3}{4}.0,05+\dfrac{1}{2}.0,2=0,0875\left(mol\right)\)
\(\Rightarrow V_{O_2\left(đktc\right)}=0,0875.22,4=1,96\left(l\right)\)

Câu 1:
Gọi số mol NaCl, KCl là a, b (mol)
=> 58,5a + 74,5b = 6,81 (1)
\(n_{AgCl}=\dfrac{14,35}{143,5}=0,1\left(mol\right)\)
Bảo toàn Cl: a + b = 0,1 (2)
(1)(2) => a = 0,04 (mol); b = 0,06 (mol)
\(\left\{{}\begin{matrix}m_{NaCl}=0,04.58,5=2,34\left(g\right)\\m_{KCl}=0,06.74,5=4,47\left(g\right)\end{matrix}\right.\)
Câu 2:
Gọi số mol MgCl2, KCl là a, b (mol)
=> 95a + 74,5b = 3,93 (1)
25ml dd A chứa \(\left\{{}\begin{matrix}MgCl_2:0,05a\left(mol\right)\\KCl:0,05b\left(mol\right)\end{matrix}\right.\)
nAgNO3 = 0,05.0,06 = 0,003 (mol)
=> nAgCl = 0,003 (mol)
Bảo toàn Cl: 0,1a + 0,05b = 0,003 (2)
(1)(2) => a = 0,01 (mol); b = 0,04 (mol)
\(\left\{{}\begin{matrix}\%m_{MgCl_2}=\dfrac{0,01.95}{3,93}.100\%=24,173\%\\\%m_{KCl}=\dfrac{0,04.74,5}{3,93}.100\%=75,827\%\end{matrix}\right.\)


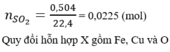
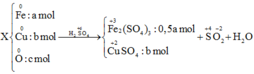
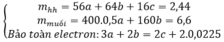
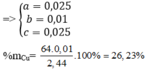
Khối lượng muối trong hỗn hợp :
Đặt x và y là số mol KCl và K 2 SO 4 trong hỗn hợp. Ta có
74,5x + 174y = 1,14 (1)
Khối lượng K 2 SO 4 sau phản ứng bao gồm khối lượng K 2 SO 4 vốn có trong hỗn hợp ban đầu và khối lượng K 2 SO 4 sinh ra sau phản ứng (m = 174.0,5x = 87x). Ta có :
87x+ 174y= 1,218 (2)
Giải hệ phương trình (1) và (2), được x = 0,006 ; y = 0,004.
Khối lượng KCl là : 74,5.0,006 = 0,447 (g).
Khối lượng K 2 SO 4 là : 1,143 - 0,447 = 0,696 (g).