Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn C.
Hỗn hợp E gồm X (3x mol); Y (2x mol); Z (3x mol)
Dung dịch Y chứa R(COONa)2: 5x mol và NaOH dư: 0,13 – 10x mol
Khi nung T với CaO thu được 1 hidrocacbon đơn giản nhất là CH4 (0,015 mol) Þ R là –CH2
và phản ứng nung T tạo CH4 tính theo mol của muối thì: 0,13 – x = 0,03 Þ x = 0,01 mol (vì nếu tính theo mol của NaOH thì nmuối < nhiđrocacbon).
Dựa vào các đáp án nhận thấy các anol đều no đơn chức nên công thức của ancol là CnH2n + 2O (n > 0)
Gọi công thức của Z là CmH2m – 4O4 (m > 4)
Khi đốt cháy X thì: 0,045n + 0,04 + 0,03.(1,5m – 2,5) = 0,28 Þ n + m = 7
+ Với n = 1 và m = 6 Þ X là CH3OH và Z là CH3OOCCH2COOC2H5
Þ Y là CH2(COOH)2 (0,02 mol) Þ %mY = 28,03%

Chọn đáp án A
Xử lý dữ kiện T:
-OH + Na → -ONa + 1/2H2
⇒ nOH = ![]() mol.
mol.
Bảo toàn khối lượng:
mT=m bình tăng +mH2=4,45 + 0,075.2=4,6
Gọi n là số gốc OH trong T
![]()
⇒ ứng với ![]()
=> T là glixerol: C3H8O3;
![]()
![]() mol
mol
=> nCOO=n NaOH phản ứng= 0,165:1,5=0,11 mol.
Giải đốt ![]() mol O2 → 0,34 mol CO2 + 0,25 mol H2O.
mol O2 → 0,34 mol CO2 + 0,25 mol H2O.
Bảo toàn khối lượng:
![]()
Bảo toàn nguyên tố oxi:
![]()
![]()
![]()
Quy E về X, Y, T, H2O
⇒ ![]() mol;
mol;
![]() mol.
mol.
TH1: X và Y là axit đơn chức.
Không mất tính tổng quát, giả sử
![]() .
.
Mà ![]() mol
mol
⇒ ![]() mol;
mol; ![]() mol.
mol.
Gọi số C trong X và Y lần lượt là x và y mol
⇒ 0,07x + 0,04y + 0,05 × 3 = 0,34
⇒ 7x + 4y = 19
→ giải phương trình nghiệm nguyên có: x = 1 và y = 3.
⇒ X là HCOOH
⇒ số H trong Y
![]()
⇒ Y là HC≡C-COOH mà ![]() mol =
mol = ![]()
Z chỉ chứa 1 gốc Y và 2 gốc X.
⇒ Z là (HCOO)2(HC≡C-COO)C3H5: 0,02 mol
⇒ %mZ trong E = 41,93%.
TH2: X là axit đơn chức và Y là axit 2 chức
→ biện luận tương tự và loại

Giải thích: Đáp án C
T là este 2 chức, mạch hở, tạo từ 2 axit và 1 ancol nên các axit này đều là đơn chức và ancol 2 chức.
Đặt Z là R(OH)2 ![]()
Khối lượng tăng là khối lượng của RO2 bị hấp thụ ![]()
thỏa mãn Z là C3H6(OH)2.
Muối có dạng RCOONa 0,4 mol
![]() thỏa mãn muối là HCOONa 0,2 mol và CxH3COONa 0,2 mol
thỏa mãn muối là HCOONa 0,2 mol và CxH3COONa 0,2 mol
![]()
Vậy X, Y là HCOOH và CH2=CH-COOH
→ T là HCOOC3H6OOC-CH=CH2.
Quy đổi E thành:
HCOOH 0,2 mol, CH2=CH-COOH 0,2 mol, C3H6(OH)2 0,26 mol và H2O –y mol
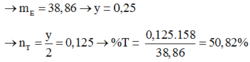

Giải thích: Đáp án C
Đốt M cho nCO2 = nH2O. Lại có đốt X và Y cho nCO2 = nH2O.
Mặt khác: T chứa ít nhất 2πC=O ⇒ k ≥ 2 ⇒ đốt cho nCO2 > nH2O
||⇒ đốt Z cho nCO2 < nH2O ⇒ Z là ancol no, 2 chức, mạch hở.
► Quy M về HCOOH, C2H4(OH)2, (HCOO)2C2H4 và CH2.
Đặt số mol các chất trên lần lượt là x, y, z và t.
mM = 3,21(g) = 46x + 62y + 118z + 14t; nKOH = 0,04 mol = x + 2z.
nCO2 = 0,115 mol = x + 2y + 4z + t; nH2O = 0,115 mol = x + 3y 3z +z.
► Giải hệ có: x = 0,02 mol; y = 0,01 mol; z = 0,01 mol; t = 0,035 mol.
Dễ thấy để có 2 axit đồng đẳng kế tiếp thì ta ghép 1CH2 vào ancol.
⇒ M gồm HCOOH: 0,015 mol; CH3COOH: 0,005 mol;
C3H6(OH)2: 0,01 mol; (HCOO)(CH3COO)C3H6: 0,01 mol.
► %mZ = 0,01 × 76 ÷ 3,21 × 100% = 23,68% ⇒ chọn C.

Đáp án B
Đặt nAncol = nCnH2n+2O = a || ∑(nY và E) = nCmH2m–2Oc = b
Ta có ∑nCO2 = an + bm = 0,09 (1)
Dựa vào PTPU cháy tổng quát: CxHyOz + (x + y/4 –z/2)O2 ta có
PT theo nO2 là: 1,5an + 1,5bm – 0,5b – 0,5bc = 0,06 (2)
● Giả sử axit Y đơn chức ⇒ c = 2 ⇒ (2) <=> 1,5an + 1,5bm – 1,5b = 0,06 mol (3)
Lấy (1)×1,5 – (2) ta có 1,5b = 0,09×1,5 – 0,06 = 0,075 ||⇒ b = 0,05 mol.
Nhận thấy an + bm = 0,09 ⇒ bm < 0,09 || mà b = 0,05
⇒ m < 0,09/0,05 = 1,8 ⇒ LOẠI vì Y bé nhất là CH2=CH–COOH.
● Giả sử axit Y 2 chức ⇒ c = 4 || LÀm tương tự ở trên ta có b = 0,03 mol
⇒ m < 0,09/0,03 = 3 ⇒ Chỉ có 1 axit thỏa mãn là (COOH)2 (axit oxalic).
Mà nKOH = 0,075 ||⇒ T chứa (COOK)2:0,03 mol và nKOH dư = 0,015 mol.
⇒ %mKOH dư = 0,015×56×100/ (0,03×166 + 0,015×56) ≈ 14,433%
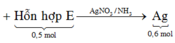
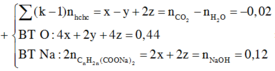
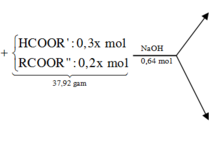
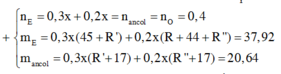
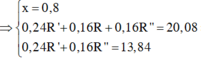
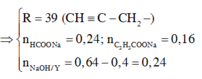



Đáp án D
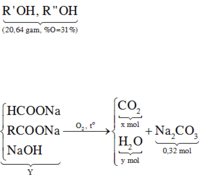
♦ Cách 1: ∑nNa = 0,96 mol ||→ NaOH cần để thủy phân là 0,8 mol → dư 0,16 mol NaOH đốt cho 0,08 mol H2O.
||→ theo đó nếu cần suy luận ra được 2 axit là (COOH)2 và HOOCC≡CCOOH (%O và mạch không nhánh).
Tuy nhiên, giải BT này ta không cần. ► Note: Sơ đồ thủy phân kết hợp đối cháy:
Gọi x là số mol CO2 khi đốt m gam chất rắn, đại diện ancol là 0,8 mol CnH2n + 2O.
Để ý: trong m gam chất rắn có 0,16 mol NaOH và 0,8 mol O2Na, bảo toàn O → nO2 cần đốt = x – 0,12 mol.
Bảo toàn O2 dùng đốt của các chất trong pt thủy phân có: 1,925 = x – 0,12 + 1,2n (1).
Đốt E, dùng BTKL có mCO2 + H2O = 114,5 gam. Xét lượng H2O và CO2 là kết quả đốt cháy
của các sp thủy phân có: 114,5 + 0,48 × 18 = 0,48 × 44 + 0,08 × 18 + 44x + (49,6n + 14,4) (2).
Giải hệ phương trình (1) và (2) được x = 0,62 mol và n = 1,1875 → mancol = 27,7 gam.
Áp dụng BTKL cho phương trình thủy phân ||→ m = 63,6 gam.
♦ Cách 2: nNaOH = 0,96 mol gồm 0,16 mol NaOH dư và 0,8 mol NaOH vừa đủ.
Quy 52,9 gam E gồm 0,8 mol COOH; x mol CH2 và y mol
C. Giải hệ khối lượng 52,9 gam và O2 cần đốt tìm ra x = 0,95 mol và y = 0,3 mol.
Lại chú ý đốt muối thu được 0,08 mol H2O vừa đúng cân bằng với 0,16 mol H trong 0,16 mol NaOH dư.
→ nghĩa là muối không chứa Natri và cần thì như cách 1 đã biện luận: (COONa) và C2(COONa)2.
→ Yêu cầu: mmuối = 0,3 × 12 + 0,8 × (44 + 23) + 0,16 × 40 = 63,6 gam.