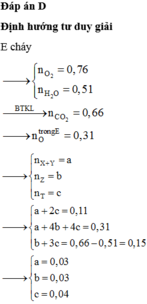Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Đốt cháy 7,48 gam hỗn hợp E cần 0,27 mol O2 thu được CO2 và H2O có số mol bằng nhau. Vậy Z phải là ancol no và số mol của Z và T bằng nhau.
BTKL: m C O 2 + m H 2 O = 7 , 48 + 0 , 27 . 32 = 16 , 12 g a m
n C O 2 = n H 2 O = 0 , 26 m o l
Bảo toàn O: n O t r o n g E = 0 , 26 . 3 - 0 , 27 . 2 = 0 , 24 m o l
Mặt khác lượng E trên tác dụng vừa đủ 0,1 mol KOH
n C O O t r o n g E = 0 , 1 → n Z = 0 , 24 - 0 , 1 . 2 2 = 0 , 02 = n T → n X + n Y = 0 , 1 - 0 , 02 . 2 = 0 , 06 m o l
Gọi n là số C của Z
→ n C ( X + Y ) = 0 , 26 - 0 , 04 . n → C - X , Y = 0 , 26 - 0 , 04 n 0 , 1
Ta có: n ≥ 2 ; C - X , Y > 1
TH1: n = 2 thì 2 gốc axit là HCOO- và CH3COO- với số mol lần lượt là 0,02 và 0,08.
Do vậy không thể có X trong E vì số mol của T đã là 0,02. (loại).
TH2: n = 3 thì 2 gốc axit là HCOO- và CH3COO- với số mol lần lượt là 0,06 và 0,04.
Vậy trong E số mol của X là 0,04; Y là 0,02, Z là C3H8O2 với số mol là 0,02 mol và T là C3H5(OOCH)(OOCCH3) 0,02 mol.
Vậy 1 sai do %Y=16,04%.
2 sai do % số mol của X=40%.