Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Trường hợp 1: Khi nhỏ từ từ axit vào dung dịch muối cacbonat, phản ứng xảy ra theo trình từ
H+ + CO32- → HCO3-
Sau đó H+còn dư + HCO3- → CO2 + H2O
=> nCO2 = nH+ – nCO32- = 0,1(x – y)
Trường hợp 2: Khi nhỏ từ từ muối cacbonat vào axit thì phản ứng tạo ra ngay CO2:
2H+ + CO32- → CO2 + H2O
nCO2 = ½ nH+ = 0,05x
Do V1 : V2 = 4 : 7
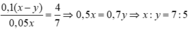

Chọn C.
T N 1 : n H + = n C O 3 2 - + n C O 2 ( T N 1 ) 0 , 1 x 0 , 1 y ? T N 2 : n H + = 2 n C O 3 2 - p ư = 2 n C O 2 ( T N 2 ) 0 , 1 x ? ? ⇒ n C O 2 ( T N 1 ) = 0 , 1 x - 0 , 1 y n C O 2 ( T N 2 ) = 0 , 05 x ⇒ 0 , 1 x - 0 , 1 y 0 , 05 x = 4 7 ⇒ x y = 7 5

Đáp án : A
Do 2 thí nghiệm tạo lượng CO2 khác nhau nên chứng tỏ HCl phải thiếu so với lượng chất trong X
+) Khi nhỏ từ từ Y vào X thì lúc đầu X rất dư nên thứ tự phản ứng sẽ là :
CO32- + H+ à HCO3-
HCO3- + H+ à CO2 + H2O
=> nCO2 = b – a = V 22 , 4
+) Khi nhỏ từ từ X vào Y thì lúc đầu Y rất dư nên các chất trong X sẽ phản ứng với axit theo tỉ lệ mol tương ứng với số mol ban đầu . Phản ứng sẽ là :
HCO3- + H+ à CO2 + H2O
, 2x à 2 x à 2 x
CO32- + 2H+ à CO2 + H2O
, x à 2x à x
=> nH+ = 4x = b và nCO2 = 3x = 3 V 22 , 4 => b = 4 V 22 , 4
=> b = 4(b – a)
=> a : b = 3 : 4

Chọn đáp án B
Chú ý : Khi cho HCl vào C O 3 2 - thì
![]()
Nhưng khi cho C O 3 2 - vào HCl thì
![]()
+ Ta có :
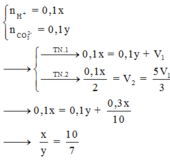

Đáp án A
Do 2 cách cho thì lượng khí CO2 thu được khác nhau nên HCl không dư.
Khi ta cho dung dịch Y từ từ vào X thì: n C O 2 = n H C l = n N a C O 3 = b - a m o l
Khi cho từ từ X tác dụng với Y thì hai muối trong X phản ứng theo tỉ lệ mol là 1:2.
Phản ứng: N a 2 C O 3 + 2 K H C O 3 + 4 H C l → 2 N a C l + 2 K C l + 3 C O 2 + 3 H 2 O
Lúc này: n C O 2 = 0 , 75 b
Từ giả thuyết suy ra: 0,75a=3(b-a)=> 3a= 2,25b=> a:b= 3:4

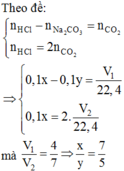


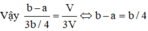


Chọn đáp án C