Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án C
C a O C l 2 + 2HCl → C a C l 2 + C l 2 + H 2 O
1 1 mol
2 K M n O 4 + 16HCl → 2KCl + 2 M n C l 2 + 5 C l 2 + 8 H 2 O
1 2,5 mol
K 2 C r 2 O 7 + 14HCl → 2KCl + 2 C r C l 3 + 3 C l 2 + 7 H 2 O
1 3 mol
M n O 2 + 4HCl → M n C l 2 + C l 2 + 2 H 2 O
1 1 mol
Vậy nếu cho cùng 1 mol mỗi chất C a O C l 2 , K M n O 4 , K 2 C r 2 O 7 , MnO2 thì K 2 C r 2 O 7 cho lượng khí C l 2 nhiều nhất.

Trong phản ứng với HCl đặc thì chất nào nhận electron nhiều nhất thì cho lượng Cl2 lớn nhất.
Giả sử có 1 mol mỗi chất CaOCl2, KMnO4, K2Cr2O7, MnO2 lần lượt phản ứng với lượng dư dung dịch HCl đặc thì số mol electron nhận lần lượt là 2 mol, 5 mol, 6 mol, 2 mol.
Vậy chất tạo ra lượng khí Cl2 nhiều nhất là K2Cr2O7. Đáp án B.

1)
| CaOCl2 | + | 2HCl | → | Cl2 | + | H2O | + | CaCl2 |
| 16HCl | + | 2KMnO4 | → | 5Cl2 | + | 8H2O | + | 2KCl | + | 2MnCl2 |
| 14HCl | + | K2Cr2O7 | → | 3Cl2 | + | 7H2O | + | 2KCl | + | 2CrCl3 |
| 4HCl | + | MnO2 | → | Cl2 | + | 2H2O | + | MnCl2 |
Theo pt:
-1mol CaOCl2 sẽ tạo ra 1mol Cl2
-1mol KMnO4 sẽ tạo ra 2,5mol Cl2
-1mol K2Cr2O7 sẽ tạo ra 3mol Cl2
-1mol MnO2 sẽ tạo ra 1mol Cl2
Vậy K2Cr2O7 tạo ra lượng khí clo nhiều nhất,CaOCl2 và MnO2 tạo ra lượng khí clo ít nhất
Theo đề, ta có: \(n_{CaOCl_2}=\dfrac{100}{127}\left(mol\right)\\ n_{KMnO_4}=\dfrac{100}{158}=\dfrac{50}{79}\left(mol\right)\\ n_{K_2Cr_2O_7}=\dfrac{100}{294}=\dfrac{50}{147}\left(mol\right)\\ n_{MnO_2}=\dfrac{100}{87}\left(mol\right)\)|
\(CaOCl_2+2HCl\rightarrow Cl_2+H_2O+CaCl_2\)
\(16HCl+2KMnO_4\rightarrow5Cl_2+8H_2O+2KCl+2MnCl_2\)
\(14HCl+K_2Cr_2O_7\rightarrow3Cl_2+7H_2O+2KCl+2CrCl_3\)
\(4HCl+MnO_2\rightarrow MnCl_2+2H_2O\)
Theo phương trình:
- \(\dfrac{100}{127}mol\) CaOCl2 sẽ tạo ra \(\dfrac{100}{127}mol\) Cl2.
- \(\dfrac{100}{158}mol\) KMnO4 sẽ tạo ra \(\dfrac{125}{79}mol\) Cl2.
- \(\dfrac{100}{294}mol\) K2Cr2O7 sẽ tạo ra \(\dfrac{50}{49}mol\) Cl2.
- \(\dfrac{100}{87}mol\) MnO2 sẽ tạo ra \(\dfrac{100}{87}mol\) Cl2.
Vậy 100(g) KMnO4 sẽ tạo ra lượng Cl2 nhiều nhất, 100(g) CaOCl2 sẽ tạo ra lượng Cl2 ít nhất.

a)
\(16HCl+2KMnO_4\underrightarrow{^{to}}5Cl_2+8H_2O+2MnCl_2\)
\(3Cl_2+6KOH\underrightarrow{^{to}}3H_2O+5KCl+KClO_3\)
\(6HCl+KClO_3\rightarrow3Cl_2+3H_2O+KCl\)
\(3Cl_2+2Fe\rightarrow2FeCl_3\)
\(FeCl_3+3KOH\rightarrow Fe\left(OH\right)_3+3KCl\)
\(KCl+NaOH\rightarrow NaCl+KOH\)
2)
\(2H_2O+CaCl_2\underrightarrow{^{đpmn}}Ca\left(OH\right)_2+Cl_2+2H_2\)
\(Cl_2+H_2\underrightarrow{^{askt}}2HCl\)
\(2HCl+Fe\rightarrow FeCl_2+H_2\)
\(2FeCl_2+Cl_2\rightarrow2FeCl_3\)
\(3Ba\left(OH\right)_2+2FeCl_3\rightarrow3BaCl_2+2Fe\left(OH\right)_3\)
3)
\(4HCl+MnO_2\underrightarrow{^{to}}Cl_2+2H_2O+MnCl_2\)
\(Cl_2+2NaOH\rightarrow H_2O+NaCl+NaClO\)
\(H_2O+NaCl+CO_2\rightarrow NaHCO_3+HClO\)
4)
\(KClO_3+3MnO_2+6NaOH\rightarrow3H_2O+KCl+3Na_2MnO_4\)
\(KCl+AgNO_3\rightarrow AgCl+KNO_3\)
\(2AgCl\underrightarrow{^{nđp,as}}2Ag+Cl_2\)
\(3Cl_2+6KOH\underrightarrow{^{to}}H_2O+5KCl+KClO_3\)
5)
\(CaOCl_2+MnSO_4+2NaOH\rightarrow H_2O+MnO_2+Na_2SO_4+CaCl_2\)
\(2CaOCl_2+H_2O+CO_2\rightarrow CaCO_3+CaCl_2+2HClO\)
\(CaCO_3\underrightarrow{^{to}}CaO+CO_2\)
\(H_2O+NaClO+CO_2\rightarrow NaHCO_3+HClO\)
6)
\(MnO_2+4HBr\rightarrow Br_2+2H_2O+MnBr_2\)
\(Br_2+2HI\rightarrow I_2+2HBr\)
\(2Ag+I_2\rightarrow2AgI\)

4HCl+MnO2-->MnCl2+2H2O+Cl2
3Cl2+2Fe-->2FeCl3
FeCl3+3NaOH-->3NaCl+Fe(OH)3
2NaCl+H2SO4-->Na2SO4+2HCl
2HCl+Cuo-->CuCl2+H2O
CuCl2+2AgNO3-->2AgCl+Cu(NO3)2

 3)
3)
3Cl2+6KOH→3H2O+5KCl+KClO3
2KClO3→2KCl+3O2
2KCl+H2SO4→K2SO4+2HCl
16HCl+2KMnO4→5Cl2+8H2O+2KCl+2MnCl2
2Ca(OH)2+2Cl2→2H2O+CaCl2+Ca(ClO)2 e)a. 2KMnO4 + 16HCl (đ) -> 2KCl + 2MnCl2 + 5Cl2 + 8H2O (Đ.C Cl2)
Cl2 + KOH -> KCl + KClO3 + H2O
2KClO3 -> 2KCl + 3O2 (đ/c khí O2 lớp 8)
2KCl -> 2K + Cl2
Cl2 + H2O ->HCl + HClO
2HCl + Fe -> FeCl2 + H2
2FeCl2 + Cl2 -> 2FeCl3
FeCl3 + NaOH -> Fe(OH)3 + NaCl

a) Giả sử lấy lượng mỗi chất là a gam
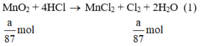
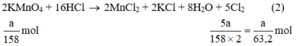
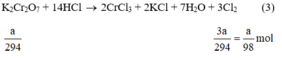
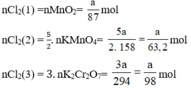
Ta có: 
Lượng Cl2 điều chế được từ pt (2) nhiều nhất.
Vậy dùng KMnO4 điều chế được nhiều Cl2 hơn.
b) Nếu lấy số mol các chất bằng a mol
Theo (1) nCl2(1) = nMnO2 = a mol
Theo (2) nCl2(2) = 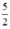 . nKMnO4 = 2,5a mol
. nKMnO4 = 2,5a mol
Theo (3) nCl2(3) = 3. nK2Cr2O7 = 3a mol
Ta có: 3a > 2,5a > a.
⇒ lượng Cl2 điều chế được từ pt (3) nhiều nhất.
Vậy dùng K2Cr2O7 được nhiều Cl2 hơn.

a/ \(14HCl+K_2Cr_2O_7\left(\frac{1}{294}\right)\rightarrow3Cl_2\left(\frac{3}{294}\right)+7H_2O+2KCl+2CrCl_3\)(1)
\(4HCl+MnO_2\left(\frac{1}{87}\right)\rightarrow Cl_2\left(\frac{1}{87}\right)+2H_2O+MnCl_2\)(2)
\(16HCl+2KMnO_4\left(\frac{1}{158}\right)\rightarrow5Cl_2\left(\frac{5}{316}\right)+8H_2O+2KCl+2MnCl_2\)(3)
\(n_{K_2Cr_2O_7}=\frac{1}{294}\)
\(\Rightarrow V_1=\frac{3}{294}.22,4=\frac{8}{35}\)
\(n_{MnO_2}=\frac{1}{87}\)
\(\Rightarrow V_2=\frac{1}{87}.22,4=\frac{112}{435}\)
\(n_{KMnO_4}=\frac{1}{158}\)
\(\Rightarrow V_3=\frac{5}{316}.22,4=\frac{28}{79}\)
\(\Rightarrow\)Vậy thể tích Cl2 thu ở phản ứng (2) là nhiều nhất
b/ Dựa vào PTHH câu a ta có:
\(n_{Cl_2\left(V_1\right)}=3.0,1=0,3\)
\(n_{Cl_2\left(V_2\right)}=0,1.1=0,1\)
\(n_{Cl_2\left(V_3\right)}=\frac{0,1.5}{2}=0,25\)
Vậy thể tích Cl2 ở phản ứng đầu là lớn nhất
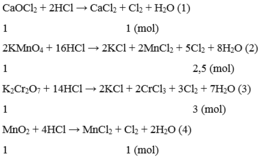

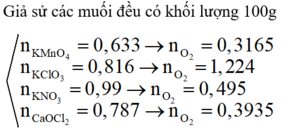

2KMnO4+ 16HCl => 2MnCl2+ 2KCl+ 5Cl2+ 8H2O
1_____________________________2.5
MnO2+ 4HCl => MnCl2+ Cl2+ 2H2O
1_____________________1
KClO3+ 6HCl => KCl+ 3Cl2+ 3H2O
1___________________3
CaOCl2 + 2HCl => CaCl2 + Cl2 + H2O
1_______________________1
=> KClO3 điều chế Cl2 nhiều nhất