Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(4Al+3O_2\xrightarrow[]{t^o}2Al_2O_3\) : Nhôm oxit
\(4Fe+3O_2\xrightarrow[]{t^o}2Fe_2O_3\) : Sắt (III) oxit
\(C+O_2\xrightarrow[]{t^o}CO_2\) : Cacbon đioxit
\(S+O_2\xrightarrow[]{t^o}SO_2\) : Lưu huỳnh đioxit
4Al + 3O2 → 2Al2O3 (đây là phản ứng hóa hợp vì chỉ có 1 chất sản phẩm)( tên : Nhôm oxit)
3Fe + 2O2 → Fe3O4 (đây là phản ứng hóa hợp vì chỉ có 1 chất sản phẩm) (tên là oxit sắt từ hoặc Sắt (2,3)oxit)bạn ghi số la mã hộ mk nha
C + O2 → CO2 (là phản ứng hóa hợp vì chỉ có 1 chất sản phẩm)(tên là cacbon đi oxit)
S + O2 → SO2(là phản ứng hóa hợp vì chỉ có 1 chất sản phẩm)(tên : lưu huỳnh đi oxit
TẤT CẢ PT TRÊN BẠN GHI THÊM NHIỆT ĐỘ K SAI NHA

a)
- Hiện tượng: Lưu huỳnh cháy trong không khí với ngọn lửa nhỏ, màu xanh nhạt; cháy trong oxi mãnh liệt hơn
S + O2 --to--> SO2 (pư hóa hợp)
Sản phẩm: Lưu huỳnh đioxit
b)
- Hiện tượng: Sắt cháy mạnh, sáng chói, tạo ra các hạt nhỏ nóng chảy màu nâu
3Fe + 2O2 --to--> Fe3O4 (pư hóa hợp)
Sản phẩm: Sắt từ oxit
a,S+O2to⟶SO2S+O2⟶toSO2 Hiện tượng :Lưu huỳnh cháy trong không khí với ngọn lửa nhỏ, màu xanh nhạt; cháy trong khí oxi mãnh liệt hơn, tạo thành khí lưu huỳnh đioxit và rất ít lưu huỳnh trioxit . Chất rắn màu vàng Lưu huỳnh dần chuyển sang thể hơi.
b,3Fe+2O2to⟶Fe3O43Fe+2O2⟶toFe3O4 Hiện tượng :Khi mẩu than cháy trước tạo nhiệt độ đủ cao cho sắt cháy. Sắt cháy mạnh, sáng cói, không có ngọn lửa, không có khói, tạo ra các hạt nhỏ nóng chảy màu nâu là sắt (II, III) oxit, công thức hoá học là Fe3O4 thường được gọi là oxit sắt từ. Màu trắng xám của Sắt dần chuyển sang màu nâu thành hợp chất Oxit sắt từ.

\(S+O_2\rightarrow\left(t^o\right)SO_2\\ 4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\\ 2Mg+O_2\rightarrow\left(t^o\right)2MgO\)
Đọc tên sản phẩm:
SO2 : Lưu huỳnh dioxit
Al2O3: Nhôm oxit
MgO: Magie oxit

\(C+O_2\underrightarrow{t^0}CO_2\) ( Cacbon dioxit)
\(4P+5O_2\underrightarrow{t^0}2P_2O_5\)( Diphotpho pentaoxit)
\(H_2+\dfrac{1}{2}O_2\underrightarrow{t^0}H_2O\) ( Nước hay dihidro monooxit)
\(4Al+3O_2\underrightarrow{t^0}2Al_2O_3\) ( Nhôm oxit)

C + O2 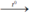 CO2. Cacbon đioxit.
CO2. Cacbon đioxit.
4P + 5O2 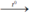 2P2O5. Điphotpho pentaoxit.
2P2O5. Điphotpho pentaoxit.
2H2 + O2 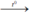 2H2O. Nước.
2H2O. Nước.
4Al + 3O2 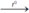 2Al2O3. Nhôm oxit.
2Al2O3. Nhôm oxit.

a/ 2Al + 3S -to-> Al2S3
b/ Fe + S -to-> FeS
c/ Pb + S -to-> PbS
d/ 2Na + S -to-> Na2S
a/ 2Al + 3S -to-> Al2S3
b/ Fe + S -to-> FeS
c/ Pb + S -to-> PbS
d/ 2Na + S -to-> Na2S

Các oxit tác dụng với nước: N a 2 O , P 2 O 5 , C O 2 , S O 3
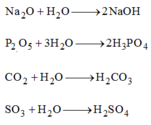
- Các oxit không hòa tan trong nước: CuO, MgO, A l 2 O 3 .

Bài 8:
\(V_{O_2}=20.100=2000\left(ml\right)=2\left(l\right)\\ a,PTHH:2KMnO_4\rightarrow\left(t^o\right)K_2MnO_4+MnO_2+O_2\\ n_{O_2}=\dfrac{2}{22,4}=\dfrac{5}{56}\left(mol\right)\\ n_{O_2\left(p.ứ\right)}=\dfrac{5}{56}.90\%=\dfrac{9}{112}\left(mol\right)\\ n_{KMnO_4\left(dùng\right)}=\dfrac{9}{112}.2=\dfrac{9}{56}\left(mol\right)\\ \Rightarrow m_{KMnO_4}=\dfrac{9}{56}.158=\dfrac{711}{28}\left(g\right)\\ b,2KClO_3\rightarrow\left(t^o,xt\right)2KCl+3O_2\\ n_{KClO_3}=\dfrac{2}{56}.\dfrac{2}{3}=\dfrac{1}{42}\left(mol\right)\\ m_{KClO_3}=122,5.\dfrac{1}{42}=\dfrac{35}{12}\left(g\right)\)
Bài 1:
\(C+O_2\rightarrow\left(t^o\right)CO_2\)
Tên sản phẩm: Cacbon dioxit/ Khí cacbonic
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
Tên sản phẩm: Điphotpho pentaoxit
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
Tên sản phẩm: Nước
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Tên sản phẩm: Nhôm oxit
\(Na+O_2-^{t^o}\rightarrow Na_2O\left(Natrioxit\right)\\ 4P+5O_2-^{t^o}\rightarrow2P_2O_5\left(Điphốtphopentaoxit\right)\\ 4Al+3O_2-^{t^o}\rightarrow2Al_2O_3\left(Nhômoxit\right)\)
Tất cả phản ứng trên đều thuộc loại phản ứng hóa hợp