Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Các phương trình điều chế HNO3 từ NH3
4NH3 + 5O2 ![]() 4NO + 6H2O
4NO + 6H2O
2NO + O2→2NO2
4NO2 + O2 + 2H2O→ 4HNO3
Theo bảo toàn nguyên tố N ta có:
nHNO3=nNH3=112 000/22,4=5000 mol
→mHNO3=315 000 gam= 315 kg
→ mddHNO3= 315.100/60=525 kg
Do hiệu suất bằng 80% nên mddHNO3 thực = mPT.80/100= 525.80/100=420 kg

- Đáp án A
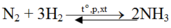
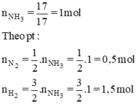
Do hiệu suất 25% nên
nN2cần dùng = 2( mol) và nH2cần dùng = 6(mol).
⇒VN2 = 2. 22,4 = 44,8 (lit) và VH2 = 22,4. 6= 134,4 (lit).

Đáp án A
Theo bảo toàn nguyên tố N ta có;
nHNO3= nNH3= 2 mol → mHNO3=126 gam
Do hiệu suất mỗi phản ứng lần lượt là 60%; 50%; 80% nên
mHNO3 thực tế thu được= 126. 60%.50%.80%= 30,24 gam

PTHH:3H2+N2=2NH3
nNH3=0,2(mol) suy ra nH2=0,3(mol);nN2=0,1(mol)
suy ra V H2=6,72(l);V N2=2,24(l)
mà hiệu suất phản ứng chỉ có 20 phần trăm
suy ra V H2 cần dùng để điều chế 4,48 lít NH3 là:6,72x100:20=3,36(l)
V N2 cần dùng để điều chế 4,48 lít NH3 là:2,24x100:20=11,2(l)

$N_2 + 3H_2 \buildrel{{t^o,xt,p}}\over\rightleftharpoons 2NH_3$
Ta thấy : $V_{N_2} : 1 > V_{H_2} : 3$ nên $N_2$ dư
Gọi hiệu suất là a
Suy ra : $V_{H_2\ pư} = 11,2a(lít)$
$V_{N_2\ pư} = \dfrac{11,2a}{3}$
$V_{NH_3} = \dfrac{2.11,2a}{3} $
Ta có :
$11,2 - 11,2a + 6,72 - \dfrac{11,2a}{3} + \dfrac{2.11,2a}{3} = 13,44$
$\Rightarrow a = 0,6 =6 0\%$

Đáp án A
Ta có: C 2 H 2 + H 2 O → C H 3 C H O
G ọ i n C 2 H 2 p h ả n ứ n g = a ( m o l ) ⇒ n C H 3 C H O = a ( m o l ) ; n C 2 H 2 d ư = 0 , 25 - a ( m o l )
Khi cho khí A vào dung dịch AgNO3 dư trong NH3 thì kết tủa tạo thành là Ag và
AgC ≡ CAg
n A g = 2 n C H 3 C H O = 2 a ( m o l ) ; n C 2 A g 2 = n C 2 H 2 d ư = 0 , 25 - a ( m o l ) ⇒ m A g + m C 2 A g 2 = 2 a . 108 + ( 0 , 25 - a ) . 240 = 56 , 4 ( g ) ⇒ a = 0 , 15 ( m o l ) V ậ y H = 0 , 15 0 , 15 = 60 %

Chọn đáp án B
Ta có 6,2 kg = 6200 g
+ Ta có 1P → 1H3PO4.
⇒ nH3PO4 = nP × 0,8
= 6200 × 0,8 ÷ 31
= 160 mol.
⇒ VH3PO4 = 160 ÷ 2 = 80 lít
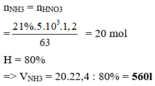
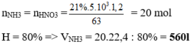
Đáp án C.