Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
$m_{O\ trong\ oxit} = 40,6 - 26,2 = 14,4(gam)$
$n_O = \dfrac{14,4}{16} =0,9(mol)$
$2H^+ + O^{2-} \to H_2O$
$n_{HCl} = n_{H^+} = 2n_O = 1,8(mol)$
$\Rightarrow V = \dfrac{1,8}{0,5} = 3,6(lít)$
b) $n_{Cl} = n_{HCl} = 1,8(mol)$
$m_{muối} = m_{kim\ loại} + m_{Cl} = 26,2 + 1,8.35,5 = 90,1(gam)$

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Bảo toàn khối lượng: m oxit + m HCl = m muối + m H 2 O
⇒ 20,3 + 0,9.36,5 = m muối + 0,45.18
⇒ m muối = 45,05g

Ta có sơ đồ chuyển hoá :
Mg, Zn, Al → O 2 MgO, ZnO, Al 2 O 3
MgO + 2HCl → MgCl 2 + H 2 O
ZnO + 2HCl → ZnCl 2 + H 2 O
Al 2 O 3 + 6HCl → 2 AlCl 3 + 3 H 2 O
MgO, ZnO, Al 2 O 3 → HCl MgCl 2 , ZnCl 2 , AlCl 3
Ta có khối lượng O 2 đã phản ứng : m O 2 = 20,3 - 13,1 = 7,2 (g)
Vậy khối lượng oxi trong hỗn hợp oxit là 7,2 gam.
Toàn bộ lượng oxi trong oxit đã chuyển vào H 2 O nên ta có m O ( H 2 O ) = 7,2g
Cứ 1 mol H 2 O thì chứa 1 mol nguyên tử O ⇒ n H 2 O = n O = 7,2 : 16 = 0,45 mol
Từ phương trình ta có:
n HCl = 2 n H 2 O = 2.0,45 = 0,9 mol
⇒ V HCl = 0,9/0,4 = 2,25l

Chọn C
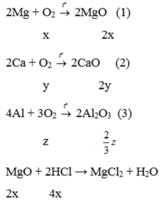

Áp dụng định luật bảo toàn khối lượng cho PT (1), (2), (3), ta có:
![]()
![]()
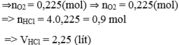

Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.


\(a,n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ 2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow n_{Al}=0,2(mol)\\ \Rightarrow m_{Al}=0,2.27=5,4(g)\\ b,m_{hh}=5,4+12,8=18,2(g)\\ c,n_{HCl}=0,6(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,6}{0,3}=2M\)
a) \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: 2Al + 6HCl --> 2AlCl3 + 3H2
_____0,2<----0,6<---------------0,3
=> mAl = 0,2.27 = 5,4(g)
b) mhh = 5,4 + 12,8 = 18,2(g)
c) \(C_{M\left(HCl\right)}=\dfrac{0,6}{0,3}=2M\)

Khối lượng O2 phản ứng = mOxit - mKim loại = 40,6-26,2=14,4
nO2=14,4 : 32= 0,45,ol
vì nHCl = 2nO2 => nHCl = 0.9mol
vậy VHCl = 0,9 : 0,5 = ? lít
k nha ( ͡❛ ‿‿ ͡❛)

Giả sử hỗn hợp chỉ chứa : Mg
\(n_{Mg}=\dfrac{6.5}{24}=0.27\left(mol\right)\)
\(n_{HCl}=0.3\cdot2=0.6\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(0.27.........0.54\)
\(n_{HCl}=0.54< 0.6\)
=> A tan hết .
\(2.\)
\(n_{Fe}=n_{Mg}=a\left(mol\right),n_{Zn}=b\left(mol\right)\)
\(n_{hh}=2a+b=0.15\left(mol\right)\)
\(m_{hh}=80a+65b=6.5\left(g\right)\)
\(\Rightarrow a=0.065,b=0.02\)
\(\%Fe=\dfrac{0.065\cdot56}{6.5}\cdot100\%=56\%\)
\(\%Mg=\dfrac{0.065\cdot24}{6.5}\cdot100\%=24\%\)
\(\%Zn=20\)