Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
VX = 0,3 lit
=> Thể tích mỗi dung dịch axit thành phần là 0,1 lit
=> nH+ = nHCl + 2nH2SO4 + 3nH3PO4 = 0,1.0,3 + 2.0,1.0,2 + 3.0,1.0,1 = 0,1 mol
Để trung hòa thì : nH+ = nOH- = 0,1 mol
Có : nOH- = nNaOH + 2nBa(OH)2 = (0,2 + 0,1.2).V.10-3 = 0,1 mol
=> V = 250 ml

Đáp án A
nH+= nHCl+ 2nH2SO4+ 3nH3PO4= 0,1.0,3+ 2.0,2.0,1+ 3.0,1.0,1=0,1 mol
nOH-= (V.0,1+2.0,2.V)/1000 mol
H+ + OH-→ H2O
Theo PT: nH+= nOH- nên 0,1=(V.0,1+2.0,2.V)/1000 suy ra V= 200 ml

Câu 15 :
$n_{HCl} = 0,2.0,1 = 0,02(mol)$
$n_{H_2SO_4} = 0,2.0,05 = 0,01(mol)$
$\Rightarrow n_{H^+} = 0,02 + 0,01.2 = 0,04(mol)$
$n_{OH^-\ dư} = 0,5.(10-14 : 10-13) = 0,05(mol)$
$H^+ + OH^- \to H_2O$
$n_{OH^-} = 0,04 + 0,05 = 0,09(mol)$
$n_{Ba(OH)_2} = \dfrac{1}{2}n_{OH^-} = 0,045(mol)$
$a = 0,045 : 0,3 = 0,15(M)$
$Ba^{2+} + SO_4^{2-} \to BaSO_4$
$n_{Ba^{2+}} = 0,045 > n_{SO_4^{2-}} = 0,01$ nên $Ba^{2+}$ dư
n BaSO4 = n SO4 = 0,01(mol)
=> m = 0,01.233 = 2,33(gam)
Đáp án A

Đáp án B
nOH- = 0,1.2.0,1 + 0,1.0,1 = 0,03
nH+ = 0,4.2.0,0375 + 0,4.0,0125 = 0,035
⇒ Trong X có H+ dư
⇒ nH+/X =0,035 – 0,03 = 0,005; VX = 100 + 400 = 500ml
⇒ [H+] = 0,01 ⇒ pH = 2.

- Trong 300 ml dung dịch X:
\(\text{nHCl = 0,3.0,3 = 0,09 mol}\)
\(\text{nH2SO4 = 0,2.0,3 = 0,06 mol}\)
\(\text{nH3PO4 = 0,1.0,3 = 0,03 mol}\)
-Trong V ml dung dịch Y chứa:
\(\text{nNaOH = 0,1.0,001V = 0,0001V (mol)}\)
\(\text{nBa(OH)2 = 0,2.0,001V = 0,0002V (mol)}\)
Phản ứng trung hòa tổng quát: b HaX + a M(OH)b → MaXb + ab H2O
Từ pư tổng quát ta thấy: nH = nOH
\(\text{+ BTNT "H": nH = nHCl + 2nH2SO4 + 3nH3PO4}\)
\(\text{+ BTNT "OH": nOH = nNaOH + 2nBa(OH)2}\)
=> nHCl + 2nH2SO4 + 3nH3PO4 = nNaOH + 2nBa(OH)2
=> 0,09 + 2.0,06 + 3.0,03 = 0,0001V + 2.0,0002V
=> V = 600 ml
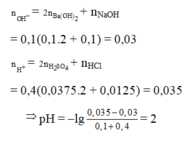
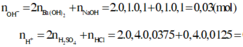
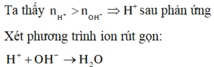
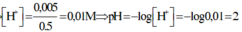
\(n_{H^+}=0.3\cdot0.1\cdot2+0.3\cdot0.15=0.105\left(mol\right)\)
\(n_{OH^-}=0.001V\cdot0.3+0.001V\cdot2\cdot0.1=0.0032V\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(0.105.......0.105\)
\(n_{OH^-\left(dư\right)}=0.0032V-0.105\left(mol\right)\)
\(\left[OH^-\right]=\dfrac{0.0032V-0.105}{0.3+0.001V}\left(M\right)\)
\(pH=14+log\left[OH^-\right]=12\)
\(\Leftrightarrow log\left[OH^-\right]=-2\)
\(\Leftrightarrow log\left[\dfrac{0.0032V-0.105}{0.3+0.001V}\right]=-2\)
\(\Leftrightarrow V=33.85\left(ml\right)\)
nH+=0,3.0,1.2+0,3.0,15=0,105 mol
nOH- ban đầu =0,3V + 0,1.2V=0,5V mol
Sau phản ứng thu được dung dịch có pH=12
⇒OH- dư ⇒ pOH=2
⇒ [OH- ] dư = 0,01 M
nOH- dư = 0,01(0,3+V)=0,003+0,01V (mol)
nOH- phản ứng=nOH- ban đầu - nOH- dư
= 0,5V - 0,003 - 0,01V
= 0,49V - 0,003 (mol )
H+ + OH- → H2O
0,105 → 0,105
nOH- phản ứng = nH+
⇒0,49V - 0,003 =0,105
⇒ V≃0,22 lít=200ml