Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Trong hỗn hợp Y: Đặt
![]()
Vì SO2 dư nên kết tủa Z gồm BaSO4 và BaSO3
Ta có:
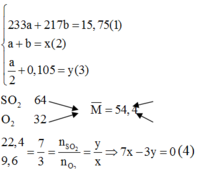


Đáp án A
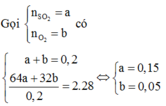
Có: ![]()
Mol trước phản ứng 0,15 0,05
Mol phản ứng 2x x 2x
Mol cân bằng (0,15 – 2x) (0,05 – x) 2x
Do đó
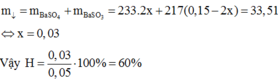

Đáp án A
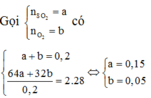
Có: ![]()
Mol trước phản ứng 0,15 0,05
Mol phản ứng 2x x 2x
Mol cân bằng (0,15 – 2x) (0,05 – x) 2x
Do đó
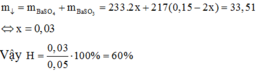

Chọn đáp án B
2SO2 + O2 ⇄ SO3 ∆ H < 0. Đây là phản ứng thuận tỏa nhiệt hay nghịch thu nhiệt.
Muốn tăng hiệu suất ta phải làm cho cân bằng dịch sang phải.Do đó phải :
Giảm nhiệt độ (loại 2)
Giảm nồng độ SO3 (loại 4)
Tăng nồng độ O2 và SO2
Tăng xúc tác thật ra yếu tố này không cần thiết vì chất xúc tác không thay đổi trong quá trình phản ứng

Đáp án C
Gọi n SO 2 = x ⇒ n O 2 = 4 x ( mol )
Phương trình phản ứng:
2SO2 + O2 D 2SO3
Ban đầu x 4x
Phản ứng: a à 0,5a à a
Cân bằng: (x-a) (4x-0,5a) a
Ta có:
% V SO 3 = a 5 x - 0 , 5 a = 4 9 ⇒ x = 0 , 55 a ⇒ H = 55 %

Đáp án C.
Gọi x là số mol oxi đã phản ứng, ta có:
Tổng số mol khí trước phản ứng là: 3 + 2 = 5 mol
Tổng số mol khí sau phản ứng là: 5 – x
![]()
Xét tỉ lệ giữa số mol và hệ số cân bằng của SO2 và O2, SO2 hết, O2 dư
![]()




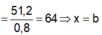
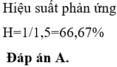
Đáp án D
n O 2 = 0 , 9 ( m o l ) , n S O 2 = 0 , 8 ( m o l )
n sau phản ứng là:
1,7-x = 1,7 – x
=> x = 0,25 (mol)