Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án D
Vì nCO2 – nH2O = 5nEste ⇒ ∑ liên kết π trong este = 5+1 = 6.
⇒ Số liên kết π/C=C = 6 – 3 = 3 ⇒ Este + Br2 tối đa theo tỷ lệ 1:3
Mà nBr2 = 72 160 = 0,45 ⇒ nEste = 0 . 45 3 = 0,15 mol
Bảo toàn khối lượng ta có mEste = 110,1 – 72 = 38,1 gam.
⇒ Tăng giảm khối lượng ta có mMuối = mEste + mK – mC3H5
mMuối = 38,1 + 0,45×39 – 0,15×41 = 49,5 gam ⇒ Chọn D

Đáp án A
Ta có:
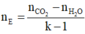
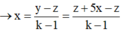
![]()
Trong E có 6 liên kết π (3 liên kết π của gốc R và 3 liên kết π của 3 nhóm COO)
![]()
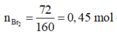
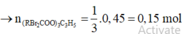
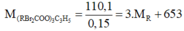
![]()
![]()
![]()
![]()

Đáp án A.
Đặt công thức của este E là (RCOO)3C3H5
Ta có y = z + 5x → y –z = 5x
→E có 6 liên kết pi (3 pi trong gốc COO, 3 pi trong gốc hiđrocacbon)
![]()
![]()
![]()
![]()

Chọn đáp án A
Có b-c = 6a → chứng tỏ X chứa 7 liên kết π = 3πCOO + 4πC=C
Cứ a mol X tác dụng vừa đủ với 4a mol Br2 → nX = 0,08 : 4 = 0,02 mol
Bảo toàn khối lượng → mX = 18,12 - 0,08. 160 = 5,32 gam
X + 3NaOH → muối + C3H5(OH)3
Có nNaOH = 0,02. 3 = 0,06 mol và nC3H5(OH)3 = 0,02 mol
bảo toàn khối lượng → m = 5,32 + 0,06. 40 - 0,02. 92 = 5,88 gam.

Chọn đáp án B
♦ giải đốt a gam E dạng CnHmO6 + 0,21 mol O2 → t o 0,2 mol CO2 + 0,14 mol H2O.
BTKL có a = mE = 4,6 gam và bảo toàn nguyên tố O có nE = 1/6.∑nO trong E = 0,02 mol.
♦ Thủy phân: 4,6 gam E + 0,02 × 3 mol NaOH → b gam muối + 0,02 mol C3H5(OH)3.
BTKL có b = mmuối = 4,6 + 0,06 × 40 – 0,02 × 92 = 5,16 gam

Chọn đáp án D
► Đối với HCHC chứa C, H và có thể có O thì:
nCO2 – nH2O = (k – 1).nHCHC (với k là độ bất bão hòa của HCHC).
► Áp dụng: b – c = 4a ⇒ k = 5 = 3πC=O + 2πC=C.
⇒ nX = nH2 ÷ 2 = 0,15 mol || Bảo toàn khối lượng:
m1 = 36,9 – 0,3 × 2 = 36,3(g) || nNaOH = 3nX = 0,45 mol.
nglixerol = nX = 0,15 mol. Bảo toàn khối lượng:
||⇒ m2 = 36,3 + 0,45 × 40 – 0,15 × 92 = 40,5(g)

Chọn A
T là este của X, Y với Z nên X cũng đơn chức.
Muối E gồm XCOONa và YCOONa
→ n(XCOONa) = n(CO2) – n(H2O) = 0,06
Trong 6,9 gam M đặt:
X là CnH2n-2O2 ( u mol)
T là CmH2m-4O4 (v mol)
→ u + v = 0,06 1
m(M) = u14n + 30) + v14m + 60) = 6,9 2
Trong phản ứng đốt cháy:
n(X) + 2n(T) = n(CO2) – n(H2O) = 0,03
→ n(O) = 2n(X) + 3n(T) = 0,06
Áp dụng ĐLBT nguyên tố O → n(O2) = 0,105
Áp dụng ĐLBT khối lượng → m(M) = 2,3 → Trong phản ứng xà phòng hóa đã dùng lượng M nhiều gấp 6,9/2,3 = 3 lần phản ứng cháy.
→ n(CO2) = (nu + mv)/3 = 0,1 3
Giải 12 và 3 → u = 0,03; v = 0,03
nu+ mv = 0,3
→ n +m = 10
Do n ≥ 3 và m ≥ 6 và m≥ n + 3 → n = 3; m = 7 là nghiệm duy nhất.
X là CH2=CH-COOH 0,03)
T là CH2=CH-COO-CH2-CH2-OOC-CH30,03)
→%T = 68,7%

Chọn đáp án C
Nhận thấy b-c= 4a → trong X có 5 liên kết π trong đó có 3 liên kết π ở gốc COO và 2 liên kết π ở gốc hidrocacbon C=C
Như vậy để hidro hóa hoàn toàn 1 mol X cần dùng 2 mol H2 → nX = 0,18 : 2 = 0,09 mol
Bảo toàn khối lương → mX = 77,58 - 0,18. 2= 77,22 gam
Khi tham gia phản ứng thủy phân → nC3H5(OH)3 = nX = 0,09 mol
Bảo toàn khối lượng → mchất rắn = mX + mKOH - mC3H5(OH)3
→ mchât rắn = 77,22 + 0,3. 56 - 0,09. 92 = 85,74 gam.
Từ b-d = 5a → A có 6 liên kết π
⟶ Gốc có 3 liên kết π ⟶A + 3Br2 = 110,1 g
⟶mA =110,1 -72 .
Dùng bảo toàn với KOH tính được x = 49,5
Đáp án B