Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
Hướng dẫn giải:
Khối lượng dung dịch H3PO4 là mdung dịch= V. D=100. 1,25= 125 gam
→ mH3PO4= 125.31,36/100= 39,2 gam → nH3PO4= 0,4 mol
Bảo toàn nguyên tố P ta có: nP= nH3PO4= 0,4 mol → mP= 12,4 gam

Đáp án B
Hướng dẫn
![]()
Theo phương trình: nC2H5OH = 0,1 mol.
Mà H = 62,5%
→ nC2H5OH = 0,1 : 62,5% = 0,16 mol.
→ mC2H5OH = 0,16 x 46 = 7,36 gam
→ VC2H5OH = 7,36 : 0,8 = 9,2 ml.
Ta có rượu 92o → Vrượu = 9,2 : 92% = 10 ml

Đáp án: B
C2H5OH -> C2H4 + H2O
n(C2H4) = 2,24 / 22,4 = 0,1 (mol) = số mol C2H5OH nguyên chất trên lý thuyết.
Trên thực tế hiệu suất phản ứng là 62,5%
=> n(C2H5OH) (lượng thực tế) = 0,1 / (62,5%) = 0,16 (mol)
=> m(C2H5OH) = 7,36 (g)
d = 0,8 (g/ml) => thể tích C2H5OH nguyên chất cần dùng là
V = 7,36 / 0,8 = 9,2(ml)
Độ của rượu được tính bằng số ml rượu nguyên chất trong 100ml dung dịch rượu.
Áp dụng điều này => cứ 100ml dung dịch rượu 92 độ có 92ml rượu nguyên chất.
Vậy để có 9,2 ml rượu nguyên chất cần thể tích dd rượu là V = 10ml.

Đáp án: B
CH3CH2OH
→
H
2
S
O
4
đ
,
170
o
C
CH2=CH2 + H2O
Theo phương trình: nC2H5OH = 0,1 mol.
Mà H = 62,5% → nC2H5OH = 0,1 : 62,5% = 0,16 mol.
→ mC2H5OH = 0,16 x 46 = 7,36 gam → VC2H5OH = 7,36 : 0,8 = 9,2 ml.
Ta có rượu 92o → Vrượu = 9,2 : 92% = 10 ml

H chung = 80%.70%.62,5% = 35%
nC2H4 → -(CH2 – CHCl-)n
Phương trình: 28n → 62,5n (tấn)
Đề bài: x ← 1 (tấn)
x = 1.28n/62,5n = 0,448 tấn = 488kg
V C2H4 = 448 : 28 . 22,4 = 368,4 m3
H = 35% ⇒ V C2H4 cần dùng = 368,4 : 35% = 1024 m3
Đáp án B.

Vì hiệu suất là 25%
=> \(m_{NH_3}=17.\dfrac{25\%}{100\%}=4,25\left(g\right)\)
Ta có: \(n_{NH_3}=\dfrac{4,25}{17}=0,25\left(mol\right)\)
PTHH: N2 + 3H2 ---> 2NH3
Theo PT: \(n_{H_2}=\dfrac{3}{2}.n_{NH_3}=\dfrac{3}{2}.0,25=0,375\left(mol\right)\)
=> \(V_{H_2}=0,375.22,4=8,4\left(lít\right)\)
Theo PT: \(n_{N_2}=\dfrac{1}{2}.n_{NH_3}=\dfrac{1}{2}.0,25=0,125\left(mol\right)\)
=> \(V_{N_2}=0,125.22,4=2,8\left(lít\right)\)
\(n_{NH_3}=1\left(mol\right)\)
Bảo toàn nguyên tố:
\(\left\{{}\begin{matrix}n_{N_2}=\dfrac{n_{NH_3}}{2}=0,5\left(mol\right)\\n_{H_2}=\dfrac{3n_{NH_3}}{2}=1,5\left(mol\right)\end{matrix}\right.\)
Do hiệu suất 25% \(\Rightarrow\left\{{}\begin{matrix}n_{N_2}=2\left(mol\right)\\n_{H_2}=6\left(mol\right)\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}V_{N_2}=44,8\left(l\right)\\n_{H_2}=134,4\left(l\right)\end{matrix}\right.\)

Để điều chế etilen người ta đun nóng ancol etylic 95 độ với dung dịch H2 SO4 đặc ở 170 độ c, hiệu suất phản ứng đạt 60,5% D rượu nguyên chất = 0,8 g g/l. Thể tích ancol 95 độ C cần đưa vào phản ứng để thu được 2,24 lít khí etilen (đktc) là bao nhiêu ml?
---
Bài làm:
nC2H4= 0,1(mol)
PTHH: C2H5OH ---H2SO4đ,170oC ---> C2H4 + H2O
0,1_____________________________0,1(mol)
nC2H5OH= nC2H4= 0,1(mol)
=> mC2H5OH= 0,1.46=4,6(g)
=> mC2H5OH(TT)= 4,6/60,5%=920/121(g)
=> VddC2H5OH( TT nguyên chất)= 920/121 : 0,8=1150/121(ml)
=> VddC2H5OH(95o)= 1150/121 : 95%\(\approx\) 10,004(ml)
----
Nguyễn Thị Thuỳ Linh Em bị tính sai nhé! Là 60,5% chứ không phải 60%? Với sao mC2H5OH(thực tế) lại bằng 46/60% nhỉ? Không phải 4,6/60,5% à?

Phương trình phản ứng:
2CH2=CH2 + O2 → 2CH3CHO (1)
Hỗn hợp X gồm: CH2=CH2 và CH3CHO
CH3CHO + H2O + 2AgNO3 + 3NH3 → CH3COONH4 + 2Ag↓ + 2NH4NO3 (2)
Theo phương trình (2):

nC2H4 ban đầu = nC2H4 pư + nC2H4 trong X = 0,075 + 0,025 = 0,1 mol
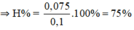

Đáp án B
Hướng dẫn CH2 = CH2 + 0,5 O2 → x t , t o CH3 – CHO
0,1 mol 0,1 mol
CH3CHO + 0,5 O2 → x t , t o CH3 – COOH
0,1 mol 0,1 mol
Số mol CH3COOH : n C H 3 C O O H = 6 60 = 0,1 mol
Thể tích etilen: V C 2 H 4 = 0,1.22,4 = 2,24 (lít)