Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Ta có PTHH
C + O2 \(\rightarrow\) CO2
mC(phản ứng) = 1 . 95% = 0.95 (tấn)
theo PT: 32g O2 : 12g C
theo ĐB : x tấn O2 : 0.95 tấn C
=> x = 0.95 x 32 : 12 =2.533 (tấn)
vậy mO2 = 2.533 tấn
b) ta có PTHH
CH4 + 2O2 \(\rightarrow\) 2H2O + CO2
Theo PT : 16g CH4 : 64g O2
Theo ĐB : 4kg CH4 : x kg O2
=> x = 4 x 64 : 16 =16 kg O2
c) Ta cóPTHH
2H2 + O2 \(\rightarrow\) 2H2O (1)
CH4 + 2O2 \(\rightarrow\) CO2 + 2H2O (2)
CÓ:
nH2 = m/M = 8/2 = 4 (mol)
nCH4 = m/M = 2/16 =0.125(mol)
theo PT(1)=> nO2 = 1/2 . nH2 = 1/2 . 4 =2 (mol)
theo PT(2) => nO2 =2 . nCH4 = 2 x 0.125 =0.25(mol)
=> tổng nO2 = 2 + 0.25 = 2.25(mol)
=> mO2 = n . M = 2.25 x 32 =72(g)

Khối lượng C có trong 1,5 tấn than là: \(m_C=\dfrac{1,5.95}{100}=1,425\) (g)
\(n_C=\dfrac{m}{M}=\dfrac{1,425}{12}=\dfrac{19}{160}\)(mol)
PTHH: C + O2 → CO2
Theo PT: \(n_{O_2}=n_C=\dfrac{19}{160}\)
Khối lượng khí oxi cần dùng là: \(m_{O_2}=n.M=\dfrac{19}{160}.32=3,8\)(g)

Khối lượng C chứa trong 1 tấn than:
PTHH: \(C+O_2\xrightarrow[]{t^o}CO_2\)
12---32-------gam
0,96--x-------tấn
\(\Rightarrow x=\dfrac{0,96.32}{12}=2,56\left(\text{tấn}\right)\)

a) PTHH: C + O2 → CO2 ↑
Đổi: 1 tấn = 1000000 gam
Khối lượng của C trong than là: 1000000.95% = 950000 gam
Số mol của C là: 950000:12 = 79166,67 mol
Số mol của O2 = 79166,67 mol
Khối lượng ôxi cần dùng là: 79166,67 . 32 = 2533333,44 gam
b) PTHH: CH4 + 2O2 → CO2 + 2H2O
Đổi: 4 kg = 4000 gam
Số mol của CH4 = 4000:16 = 250 mol
Số mol của O2 là: 250 . 2 = 500 mol
Khối lượng của O2 là: 500 . 32 = 16000 gam

Ta có: 1 m3 = 1000 dm3 = 1000 lít
Trong 1 m3 có chứa 2% tạp chất nên lượng khí CH4 nguyên chất là:
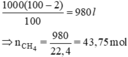
Phương trình phản ứng:
CH4 + 2O2 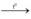 CO2 + 2H2O
CO2 + 2H2O
Từ phương trình ta có: nO2 = 2nCH4 = 2.43,75 = 87,5 mol
⇒ VO2 = 87,5.22,4= 1960 lít
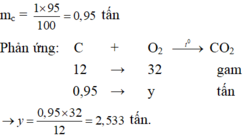
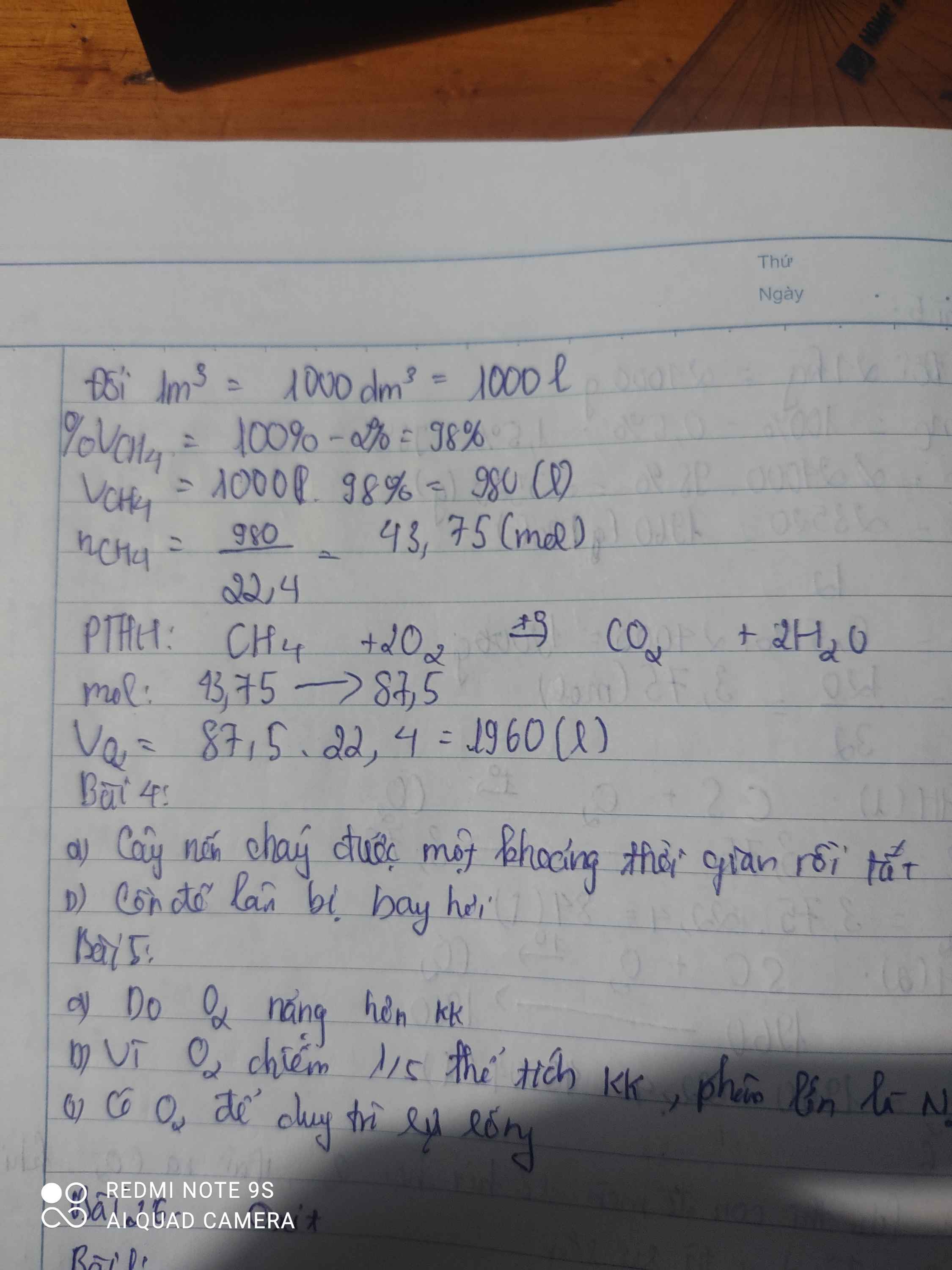
A/Khoi luong C nguyen chat=1.(95/100)=0,95 tan
C + O2---->Co2
0,95 0,95
mO2=0,95 tan
B/ CH4 + 3/2 O2---> CO2 + 2H2O
0,25 mol 0,375
mO2=12g
m