Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đặt số mol Fe2O3 = a, Số mol CuO = b, ta có 160a + 80b = 25,6
2a . 242 + b . 188 = 73,12
=> a = 0,12; b = 0,08 => nO = 0,44
=> nCO2 = 0,44
=> m = 86,68 gam
=> Đáp án B

Đáp án C
Kết tủa là CaCO3 0,05 mol do đó CO2 là 0,05 mol hay O bị khử 0,05 mol
![]()

Chọn C
Quá trình CO phản ứng với oxit chỉ là CO lấy đi O tạo CO2 nên số mol O bị lấy cũng chính bằng số mol CO2. Vì Ca(OH)2 dư ⟹ nCO2 = 34,8/100 = 0,348 = nO bị lấy
⟹ nFe trong oxit = (18,56 – 0,348×16)/56=0,232
⟹ n F e n O = 0 , 232 0 , 348 = 2 3 ⟹ Fe2O3
yCO+FexOy--t°--> yCO2+xFe
CO2+Ca(OH)2--->CaCO3+H2O nCaCO3=34,8/100=0,348(mol
Theopt2: nCO2=nCaCO3=0,348(mol)
Theo pt1:
nFexOy=1/y.nCO2=0,348/y (mol)
MFexOy=18,56/0,348/y=160y/3(g/mol)
=>56x+16y=160y/3
168x+48y=160y
168x=112y
=>x/y=112/168=2/3
Vậy công thức hoá học của Oxt sắt là Fe2O3


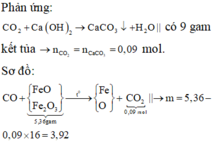
A
Ta có nO = nCaCO3 = 1,5.10-3.
Vậy m = 2,15 + 16. 1,5.10-3 = 2,174 gam