Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

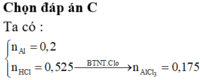
Do dd Y vẫn còn màu xanh => Cu2+ chưa điện phân hết. Gọi a là số mol đã Cu2+ điện phân.
Cu2+ + 2e ---> Cu
a............2a.........a
2H2O ---> 4H+ + O2 + 4e
.................2a.....0.5a....2a
Ta có: mgiảm = mCu + mO2
=> 64a + 0.5a*32 = 8 => a = 0.1
nCu2+ chưa đp = 0.2x - 0.1
Fe + 2H+ --->....
0.1....0.2
Fe + Cu2+ ----> Cu
0.2x-0.1.............0.2x-0.1
mFe bđầu - mFe pứ acid + mtăng do Fe + Cu2+ = mkl
=> 16.8 - 0.1*56 + 8*(0.2x - 0.1) = 12.4
=> x = 1.25
=> Đáp án D

Đáp án B
Cho Y chứa 3 kim loại, tác dụng
với dung dịch HCl dư thu được
0,035 mol khí H2 → Y chứa Fe dư
Vậy Y chứa Cu: x mol ,
Ag: x mol và Fe dư: 0,035 mol
⇒ Fe pư: 0,05 - 0,035 = 0,015 mol
Bảo toàn electron
2nCu(NO3)2 + nAgNO3 = 2nFe + 3nAl
⇒ 2x + x = 2. 0,015 + 0,03. 3
→ x = 0,04 mol
⇒ CMCu(NO3)2 = CMAgNO3
= 0,04 : 0,1 = 0,4M

ĐÁP ÁN D
nCu tạo ra = 2x; nO2 = x (bảo toàn e); 64.2x + 32x = 72;
=> x = 0,45 mol; nH+ = 4.nO2 = 1,8 mol; nCu2+ dư = y mol;
bảo toàn e: 2.nFe = 2y + 3.nNO ; nNO = 1/4.nH+ = 0,45 mol;
(1,2 - nFe).56 + 64y = 31,2; giải hệ
=> nFe phản ứng = 0,9; nCu2+ dư = y = 0,225 mol;
=> nCu2+ ban đầu = 0,9 + 0,225 = 1,125 mol;
=> a = 1,125/0,3 = 3,75 mol



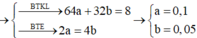
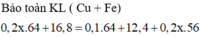





m = d∗V = d∗4πR^3 : 3
Sau khi phản xảy ra thu đương kinh viên con lại bằng
m1 = d∗V1 = d ∗ 4πR1^3 : 3
m2 = d∗V2 = d ∗ 4πR2^3 : 3
→ m1 = 8m2→ m2 = 0.7g
Khối lượng Fe phản ứng là: 5.6 - 0.7 = 4.9g
Số mol Fe tham gia pư là: 4.9/56 = 0.0875 mol
→ CM HCl = 0.0875∗20.2 = 0.875M
=> Đáp án D