Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Hỗn hợp khí sau phản ứng gồm CO dư và CO2
n hh sau = nCO (BTNT: C) = 0,2 mol
CO: 28 4 1 0,05
40 = =
CO2: 44 12 3 0,15
nCO pư = nCO2 = nO (oxit) = 0,15 mol
=> mKL = 8 – 0,15.16 = 5,6 gam

Đáp án B
![]()
=> hỗn hợp khí gồm CO2 và COdư
BTNT C=> nhh khí = nCO (bđ) = 0,3 (mol)
BTKL ta có: mCO + moxit = mKL + mhh
=> 0,3.28 + 12 = m + 40. 0,3
=> m = 8,4 (g)

nCO = 0,25
nFe = 0,1
Hỗn hợp khí thu được gồm CO dư và CO2 có M = 18,8.2 = 37,6
Bảo toàn C ta có: n CO ban đầu = n CO dư + n CO2 = 0,25
Sử dụng sơ đồ đường chéo ⇒ n CO = 0,1 mol; n CO2 = 0,15 mol
⇒ %VCO2 =( 0,15 : 0,25). 100% = 60%
Ta có: CO + Ooxit → CO2
⇒ nO/Oxit = nCO2 = 0,15 mol
⇒nFe ÷ nO = 0,1 : 0,15 = 2: 3
⇒ Oxit đó là Fe2O3
Đáp án B.

Đáp án D
Sơ đồ quá trình phản ứng:
C + H2O → hh X = {H2; CO; CO2} || X + a mol Fe3O4; b mol CuO → 25,92 gam hh Y.
(2a + 0,5b) mol H2 + hh Y → {Fe; Cu} + H2O.
Gọi số mol {CO; H2} trong X là z mol → cần đúng z mol O trong oxit đề → {CO2; H2O}.
→ 160a + 80b = 25,92 + 16z (1). Lại có để chuyển hết (3a + b) mol O trong oxit → {CO2; H2O}
thì cần vừa đủ z + 2a + 0,5b mol hh {CO; H2} → 3a + b = z + 2a + 0,5b ↔ a + 0,5b = z (2).
Từ (1) và (2) ta có z = 0,18 mol. Đến đây có 2 hướng xử lí:
cách 1: thường các bạn sẽ tìm mối ràng buộc nữa thì C + H2O → CO + H2 || C + 2H2O → CO2 + 2H2.
Bằng cách gọi số mol C ở các pt lần lượt là x, y mol → 2x + 3y = 0,2 mol
và 2x + 2y = nhh CO + H2 0,18 mol. Giải tìm ra đáp án C. ♣.
Theo hướng này có thể nhanh hơn như sau: nCO2 = 0,2 - z = 0,02 mol.
Thay vào 2 phương trình trên cũng ra kết quả tương tự.
cách 2: có thể đi theo hướng sau: hiểu rõ vấn đề + rút gọn suy nghĩ, cần hình dung:
C + H2O →....→.... cuối cùng sẽ thu được CO2 + H2O.
như vậy 0,18 mol O là ở trong CO2 luôn → có 0,09 mol C.
→ trong Y có 0,09 mol CO và CO2 (bảo toàn C) → có 0,11 mol H2O
→ mY = 0,09 × 44 + 0,11 × 18 - 0,18 × 16 = 3,06 gam. → dY/H2 = 3,06 ÷ 0,2 ÷ 2 = 7,65.
Chọn đáp án C.
p/s: bài toán này khai thác điểm đặc biệt Fe2O3 và CuO có M = 160 và 80 + bản chất CO và H2 cùng nhận 1 O.

Đáp án B
Đặt công thức oxit sắt là FexOy có số mol là a mol
Ta có: nCO= 0,2 mol
FexOy+ yCO → t 0 xFe + yCO2
a ay ax ay mol
Sau phản ứng thu được ay mol CO2, (0,2-ay) mol CO dư
M ¯ = m h h n h h = 44 . a y + 28 . ( 0 , 2 - a y ) a y + 0 , 2 - a y = 40 → a y = 0 , 15 m o l T a c ó : m F e x O y = a ( 56 x + 16 y ) = 56 a x + 16 a y = 8 g a m → a x = 0 , 1 m o l → x y = a x a y = 0 , 1 0 , 15 = 2 3 → C ô n g t h ứ c o x i t l à F e 2 O 3
Sau phản ứng thu được 0,15 mol C O 2 và 0,05 mol CO dư
→ % V C O 2 = 0 , 15 0 , 2 . 100 % = 75 %

Đáp án D
Đặt nNO = x; nN2O = y ⇒ nZ = x + y = 0,005 mol; mZ = 30x + 44y = 0,005 × 19,2 × 2.
||⇒ giải hệ có: x = 0,002 mol; y = 0,003 mol || nMg dư = nH2 = 0,005 mol
⇒ nAg = (0,336 – 0,005 × 24) ÷ 108 = 0,002 mol. Đặt nMg phản ứng = a. Bảo toàn electron:
2nMg phản ứng = 3nNO + 8nN2O + 8nNH4NO3 + nAg ⇒ nNH4NO3 = (0,25a – 0,004) mol
||⇒ mmuối = 148a + 80.(0,25a – 0,004) = 3,04(g) ⇒ a = 0,02 mol. Lại có:
ne = nH+ = nHNO3 = 4nNO + 10nN2O + 10nNH4NO3 = 0,048 mol ⇒ t = 2316(s)

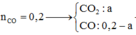
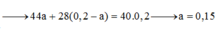
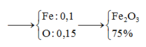

Đáp án D
Đặt công thức oxit kim loại là MxOy: a mol.
Ta có: nCO = 0,2 mol
MxOy + yCO→ x M + y CO2
a ay ax ay mol
Sau phản ứng thu được (0,2-ay) mol CO và ay mol CO2
M h h ¯ = m h h n h h = m C O + m C O 2 n C O + n C O 2 = 28 ( 0 , 2 - a y ) + 44 a y 0 , 2 - a y + a y = 20 . 2
→ ay= 0,15 mol
Ta có: moxit kim loại= a(Mx+16y)= Max+ 16ay= 8 gam
→Max = 8-16.0,15 = 5,6 gam = m