Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) \(\left\{{}\begin{matrix}\%Fe=\dfrac{56.2}{160}.100\%=70\%\\\%O=100\%-70\%=30\%\end{matrix}\right.\)
b) \(\left\{{}\begin{matrix}\%Al=\dfrac{27.2}{342}.100\%=15,79\%\\\%S=\dfrac{32.3}{342}.100\%=28,07\%\\\%O=\dfrac{16.12}{342}.100\%=56,14\%\end{matrix}\right.\)

Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.

B1 : Tìm khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B2 : Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Lập CTHH.

Các bước giải :
B1 : Tìm khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B2 : Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Lập CTHH.

\(M_{Fe_2O_3}=56.2+16.3=160\left(DvC\right)\)
\(\%Fe=\dfrac{56.2}{160}.100\%=70\%\\ \%O=100\%-70\%=30\%\)
\(M_{SO_2}=32+16.2=64\left(DvC\right)\)
\(\%S=\dfrac{32}{64}.100\%=50\%\\ \%O=100\%-50\%=50\%\)
\(M_{KHCO_3}=39+1+12+16.3=100\left(DvC\right)\)
\(\%K=\dfrac{39}{100}.100\%=39\%\\ \%H=\dfrac{1}{100}.100\%=1\%\\ \%C=\dfrac{12}{100}.100\%=12\%\\ \%O=100\%-39\%-1\%-12\%=48\%\)
Khối lượng của hợp chất Fe2O3 là:
M\(Fe_2O_3\)= 56 . 2 + 16 . 3 = 160
%mFe = \(\dfrac{112.100\%}{160}=70\%\)
%mO = 100% - 70% = 30%
__________________________________________________________________
%mS = \(\dfrac{32.100\%}{64}=50\%\)
%mO = 100 % - 50% = 50%
__________________________________________________________________
%mK = \(\dfrac{39.100\%}{100}=39\%\)
%mH = \(\dfrac{1.100\%}{100}=1\%\)
%mC = \(\dfrac{12.100\%}{100}=12\%\)
%mO = 100% - 39% - 1% - 12% = 48%
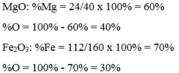
\(M_{Fe_2O_3}=56\cdot2+16\cdot3=160\left(đvc\right)\)
\(\%m_{Fe}=\dfrac{112}{160}\cdot100\%=70\%\)
\(\%m_O=\dfrac{48}{160}\cdot100\%=30\%\)
\(\left\{{}\begin{matrix}\%Fe=\dfrac{56.2}{56.2+16.3}.100\%=70\%\\\%O=100\%-70\%=30\%\end{matrix}\right.\)