
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

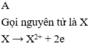

a) Từ kí hiệu ta thấy nguyên tử Ar có số đơn vị điện tích hạt nhân là 18; vậy Ar có 18 prôtn, 18 electron và có 40-18= 22 nơtron
b) Lớp vỏ electron của nguyên tử có 18e được phân bố như sau : 1s2 2s2 2p6 3s2 3p6.

Gọi số p,e,n trong của M và X lần lượt là p1,e1,n1 , p2,e2,n2
=> 2(p1+e1+n1) + ( p2+e2+n2)=140
Mà số p=số e
=> 2(2p1 + n1) + ( 2p2 + n2) = 140 <=> (4p1+2p2) + (2n1+n2)=140 (I)
Lại có : (4p1+2p2)-(2n1+n2)=44 (II)
Từ (I) và (II ) => \(\left\{{}\begin{matrix}4p1+2p2=92\left(1\right)\\2n1+n2=48\end{matrix}\right.\)
Lại có : (p1 + n1) - (p2+n2)=23 (III)
(2p1 + n1 -1) - (2p2+n2+2) =31 (IV)
Từ (III) và (IV) => \(\left\{{}\begin{matrix}p1-p2=11\left(2\right)\\n1-n2=12\end{matrix}\right.\)
Từ (1) và (2) => \(\left\{{}\begin{matrix}p1=19\\p2=8\end{matrix}\right.\)
=> số e của M là 19 e
số e của X là 8 e
=> cấu hình e của M là : 1s22s22p63s23p64s1
cấu hình e của X là : 1s22s22p4

ta có : Tổng số hạt cơ bản trong 1 nguyên tử là 95
\(\Rightarrow p+e+n=95\Leftrightarrow2p+n=95\) \(\left(1\right)\)
ta có : tỉ số giữa hạt proton + nơtron so với hạt electron là \(\dfrac{13}{6}\)
\(\Rightarrow\dfrac{p+n}{e}=\dfrac{p+n}{p}=\dfrac{13}{6}\Leftrightarrow6\left(p+n\right)=13p\)
\(\Leftrightarrow6p+6n=13p\Leftrightarrow6p+6n-13p=0\Leftrightarrow-7p+6n=0\) \(\left(2\right)\)
- từ \(\left(1\right)\) và \(\left(2\right)\) ta có hệ phương trình : \(\left\{{}\begin{matrix}2p+n=95\\-7p+6n=0\end{matrix}\right.\)
giải ra ta có : \(\left\{{}\begin{matrix}p=30\\n=35\end{matrix}\right.\) \(\Rightarrow\) kẻm \(\left(Zn\right)\)
vậy \(p=e=30\) và \(n=35\)

Hạt chứa 20 nơtron và 19 proton và 19 electron. Suy ra z = 19, số khối A = 19 + 20 = 39. Vậy hạt đó là: 3919K

Bài 2. Các hạt cấu tạo nên hầu hết các nguyên tử là
A. Proton và electron.
B. Nơtron và electron,
C. Nơtron và proton.
D. Nơtron, proton và electron.
Chọn đáp án đúng.
Chọn D.

Số đơn vị điện tích hạt nhân của nguyên tử flo là 9, suy ra flo có 9 electron phân bố vào các phân lớp như sau : ls2 2s2 2p5. Vậy flo có 5 electron ở mức năng lượng cao nhất
Số đơn vị điện tích hạt nhân là 9
=> có 9 electron trong nguyên tử flo
Electron được phân bố ở lớp vỏ như sau: 1s2 2s2 2p5
Theo trật tự các mức năng lượng obitan nguyên tử: Khi số hiệu nguyên tử Z tăng, các mức năng lượng AO tăng dần theo trình tự : 1s 2s 2p 3s 3p 4s 3d 4p 5s 4d 5p 6s 4f 5d 6p 7s 5f 6d…
=> Nguyên tử flo có 5 electron ở mức năng lượng cao nhất.

Các electron của nguyên tử nguyên tố X được phân bố trên 3 mức năng lượng, lớp thứ 3 có 6 electron, như vậy có sự phân bô” như sau: ls2 2s2 2p6 3s2 3p4
Số đơn vị điện tích hạt nhân của nguyên tử X là 16+
Các electron của nguyên tử nguyên tố X được phân bố trên 3 lớp, lớp thứ ba có 6 electron.
=> Sự phân bố electron trong nguyên tử là: 1s2 2s2 2p6 3s2 3p4 ( Lớp 1 có 1 phân lớp chứa đủ 2 e, lớp 2 có 2 phân lớp chứa đủ 8 e, lớp 3 phân lớp s chứa đủ 2e => lớp p chứa: 6 (số e lớp thứ 3) - 2 (số e phân lớp s trong lớp thứ 3) = 4e )
Vậy nguyên tử nguyên tố X có 16 electron
=> Số đơn vị điện tích hạt nhân của nguyên tử X là 16+ ( số p = số e )
Nguyên tố X là lưu huỳnh ( S )

z = 18 suy ra trong hạt nhân Ar có 18p và 22n (40 - 18), lớp vỏ electron của nguyên tử có 18e được phân bố như sau : ls2 2s2 2p6 3s2 3p6.