Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cho hh 2 muối tác dụng với H2SO4 loãng
MgCO3 + H2SO4 → MgSO4 + H2O + CO2
RCO3 + H2SO4 → RSO4 + H2O + CO2
Số mol khí CO2 sinh ra: n(CO2 1) = 4,48/22,4 = 0,2mol
Nung chất rắn không tan sau pư thấy thoát ra khí CO2 → muối cacbonat dư → H2SO4 đã tham gia phản ứng hết.
Số mol H2SO4 đã dùng: n(H2SO4) = n(CO2) = 0,2mol
Nồng độ dung dịch H2SO4: C(H2SO4) = 0,2/0,5 = 0,4M
b./ Theo ĐL bảo toàn khối lượng:
m(hh muối) + m(H2SO4) = m(muối khan) + m(B) + m(CO2) + m(H2O)
→ m(B) = m(hh muối) + m(H2SO4) - m(muối khan) - m(CO2) - m(H2O) = 115,3 + 0,2.98 - 12.2 - 0,2.44 - 0,2.18 = 110,3g
c./ Số mol CO2 thu được khi nung B: n(CO2 2) = 11,2/22,4 = 0,5mol
Tổng số mol hai muối:
n(hh muối) = n(MgCO3) + n(RCO3) = n(CO2 1) + n(CO2 2) = 0,2 + 0,5 = 0,7mol
n(RCO3) = 2,5.n(MgCO3) → n(MgCO3) = 0,2mol và n(RCO3) = 0,5mol
Khối lượng mỗi muối:
m(MgCO3) = 84.0,2 = 16,8g
m(RCO3) = m(hh muối) - m(MgCO3) = 115,3 - 16,8 = 98,5g
Khối lượng mol phân tử của muối cacbonat cần tìm:
M(RCO3) = R + 60 = m(RCO3)/n(RCO3) = 98,5/0,5 = 197
→ R = 137
Vậy kim loại cần tìm là Ba.

MgCO3+H2SO4→MgSO4+CO2+H2O
RCO3+H2SO4→RSO4+CO2+H2O
H2SO4 hết (vì X nung chỉ ra CO2)
BTKL:
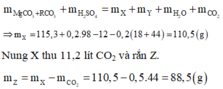
Đáp án C

Chọn đáp án C
(C17H33COO)3C3H5 + 3NaOH → 3C17H33COONa + C3H53.
+ Ta có mC17H33COONa = 30,4 ×0,75 = 22,8 gam ⇒ nC17H33COONa = 0,075 mol.
⇒ nNaOH pứ = 0,075 mol và nC3H5(OH)3 = 0,025 mol.
⇒ BTKL ta có m = 22,8 + 0,025×92 – 0,075×40 = 22,1 gam ⇒ Chọn A

Chọn đáp án C
![]()
||► Thu được rắn X ⇒ muối dư, H2SO4 hết.
⇒ nH2SO4 = nH2O = nCO2 = 0,2 mol. Bảo toàn khối lượng:
mX = 115,3 + 0,2 × 98 - 0,2 × 44 - 0,2 × 18 - 12 = 110,5(g).
Bảo toàn khối lượng: mZ = 110,5 - 0,5 × 44 = 88,5(g).

Đáp án D
Nhiệt phân thấy mhh X giảm 1,44g ⇒ mH2O tách từ bazo = 1,44g.
⇒ Quy hỗn hợp X gồm: mX = mKim loại + mO + mH2O.
Phản ứng với HCl: Đặt nO/X = a ta có:
2a + 2nH2 = nHCl ⇔ nO/X = 0,58 mol.
⇒ mKim loại trong X = m – mO – mH2O = m – 10,72 gam.
●Phản ứng với HNO3 có thể sinh ra muối NH4NO3:
Đặt nNH4NO3 = b ta có:
mMuối = m + 108,48 = mKim loại + mNO3–/Muối kim loại + mNH4NO3.
⇔ m + 108,48 + (m – 10,72) + (2nO + 3nNO + 8nNH4NO3)×62 + 80b.
⇔ m + 108,48 + (m – 10,72) + (0,58×2 + 0,2×3 + 8b)×62 + 80b ⇔ b = 0,0175 mol.
⇒ ∑nHNO3 đã pứ = 10nNH4NO3 + 4nNO + 2nO = 2,135 mol
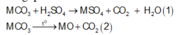
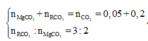
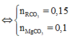
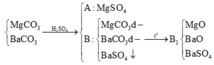

nCO2=4,4822,44,4822,4=0,2mol
MgCO3+ H2SO4 <=> MgSO4 + CO2 + H2O (1)
RCO3 + H2SO4 <=>RSO4 + CO2 +H2O (2)
Theo (1) và (2)=>nMgCO3 +nRCO3=nH2SO4=nCO2=0,2 mol
Khi nung chất rắn B còn khí CO2 thoát ra nên chứng tỏ muối cacbonat còn dư nên xảy ra 1 hoặc 2 phản ứng sau
MgCO3\to\limits^{t^o}\to\limits^{t^o}MgO + CO2 (3)
RCO3\to\limits^{t^o}\to\limits^{t^o} RO + CO2 (4)
Muối cacbonat dư nên H2SO4 hết
CMH2SO4=0,20,50,20,5=0,4M
*Theo (1) và (2) cứ 1 mol muối cacbonat chuyển thành 1 mol muối sunfat(=CO3 =SO4)
Khối lượng tăng:96-60=36g
mà có 0,2 mol muối cacbonat chuyển thành 2 mol muối sunfat nên khối lượng tăng
36.0,2=72
Theo định luật bảo toàn khối lượng có
khối lượng chất rắn B + muối(ddA)=115,3+72
=> khối lượng chất rắn B=115,3+7,2- muối khan A
mB=112,5-12=110,5
từ (3) và (4) => khối lượng C=mB -mCO2
mà nCO2=11,222,411,222,4=0,5mol
=> mCO2=0,5.44=22g
nên mC=110,5-22=88,5g
*Theo (1),(2),(3),(4),ta thấy
nMgCO3 +mRCO3=nCO2=0,2+0,5=0,7
Gọi x là số mol MgCO3 thì số mol RCO3 là 2,5x
x + 2,5x=0,7
=> 3,5x=0,7
=> x= 0,2mol
=> nMgCO3=0,2 mol
và nRCO3=0,2.2,5=0,5mol
mà mMgCO3 + mRCO3=115,3
mMgCO3=84
nên ta có 0,2.84 + 0,5(R + 60)=115,3
=> R=137 đó là kim loại Bari
a./ Các phản ứng xảy ra:
Cho hh 2 muối tác dụng với H2SO4 loãng
MgCO3 + H2SO4 → MgSO4 + H2O + CO2
RCO3 + H2SO4 → RSO4 + H2O + CO2
Số mol khí CO2 sinh ra: n(CO2 1) = 4,48/22,4 = 0,2mol
Nung chất rắn không tan sau pư thấy thoát ra khí CO2 → muối cacbonat dư → H2SO4 đã tham gia phản ứng hết.
Số mol H2SO4 đã dùng: n(H2SO4) = n(CO2) = 0,2mol
Nồng độ dung dịch H2SO4: C(H2SO4) = 0,2/0,5 = 0,4M
b./ Theo ĐL bảo toàn khối lượng:
m(hh muối) + m(H2SO4) = m(muối khan) + m(B) + m(CO2) + m(H2O)
→ m(B) = m(hh muối) + m(H2SO4) - m(muối khan) - m(CO2) - m(H2O) = 115,3 + 0,2.98 - 12.2 - 0,2.44 - 0,2.18 = 110,3g
c./ Số mol CO2 thu được khi nung B: n(CO2 2) = 11,2/22,4 = 0,5mol
Tổng số mol hai muối:
n(hh muối) = n(MgCO3) + n(RCO3) = n(CO2 1) + n(CO2 2) = 0,2 + 0,5 = 0,7mol
n(RCO3) = 2,5.n(MgCO3) → n(MgCO3) = 0,2mol và n(RCO3) = 0,5mol
Khối lượng mỗi muối:
m(MgCO3) = 84.0,2 = 16,8g
m(RCO3) = m(hh muối) - m(MgCO3) = 115,3 - 16,8 = 98,5g
Khối lượng mol phân tử của muối cacbonat cần tìm:
M(RCO3) = R + 60 = m(RCO3)/n(RCO3) = 98,5/0,5 = 197
→ R = 137
Vậy kim loại cần tìm là Ba.