Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_C=\dfrac{5000.90}{100}=4500\left(g\right)\)
=> \(n_C=\dfrac{4500}{12}=375\left(mol\right)\)
=> Nhiệt lượng tỏa ra = 375.394 = 147750 (kJ)

![]()
Trong 5 kg than có chứa 0,9.5 = 4,5 kg cacbon = 4500 gam
Số mol C = 4500 / 12 = 375 mol
=> nhiệt lượng tỏa ra = 375.394 = 147750 kJ
Đáp án: B

Nhiệt lượng toả ra khi đốt cháy hoàn toàn 1 kg etilen là :
1423/28 x 1000g = 50821,4kJ
Nhiệt lượng toả ra khi đốt cháy hoàn toàn 1 kg axetilen là :
1320/26 x 10006 = 50769,2kJ

Số mol của axetilen là :
11,2/22,4 x 20/100 = 0,1 mol
Số mol của etilen là :
11,2/22,4 x 80/100 = 0,4 mol
Vậy nhiệt lượng toả ra khi đốt là
(0,1 x 1320) + (0,4 x 1423) = 701,2 (kJ).

mC2H2 thực tế=1,4.1000=1400g
=>nC2H2=1400/26=700/13 mol
Mà đốt cháy 1 mol C2H2 nhiệt tỏa ra=432kJ
=>đốt cháy 700/13 mol C2H2 => nhiệt tỏa ra=23261,54kJ


Do lấy dư 20% oxi so với lượng cần đốt cháy nên lượng oxi đã lấy là:


Tổng khối lượng CO2 và SO2 :
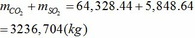
Chú ý:
Lượng O2 lấy dư 20% so với với lượng cần thiết => tính mol O2 chính xác

a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32 gam oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4 gam chất rắn. Biết khối lượng mol phân tử của oxit sắt là 160 gam/mol.
b) Chất khí sinh ra được hấp thụ hoàn toàn bằng nước vôi trong dư. Tính khối lượng kết tủa thu được.
Giải
a) Gọi CTHH của oxit sắt là: FexOy
PTHH: : FexOy + yCO ------> xFe + yCO2
Số mol Fe là

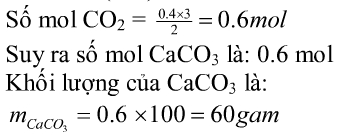
a/
mFe=22,4g
=> mO = 32-22,4=9,6g
Gọi công thức oxit sắt: FexOy
x:y=(22,4:56):(9,6:16)=2:3
=> CT: Fe2O3.
b/
nO=nC=nCO2=(9,6:16)=0,6mol
nCaCO3 =nCO2=0,6mol
=> mCaCO3 =0,6.100=60g


Khối lượng C có trong 5 kg than là:
mC =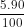 = 4,5 kg = 4500 gam
= 4,5 kg = 4500 gam
1 mol C = 12 gam
12g C cháy toả ra 394 kJ
Vậy 4500g C khi cháy toả ra x kJ
x =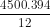 = 147750 kJ
= 147750 kJ
Khối lượng C có trong 5 kg than là:
mC =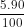 = 4,5 kg = 4500 gam
= 4,5 kg = 4500 gam
1 mol C = 12 gam
12g C cháy toả ra 394 kJ
Vậy 4500g C khi cháy toả ra x kJ
x =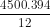 = 147750 kJ
= 147750 kJ