Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

trước tiên cho quỳ tím ẩm, lọ nào đổi màu ->màu xanh thì là nh3
3 lọ mất nhãn còn lại cho ba(oh)2 vào, đun nhẹ
+lọ chỉ có kết tủa trắng là na2so4
+lọ có sủi bọt khí (nh3) là nh4cl
+lọ vừa có kết tủa trắng vừa có sủi bọt khí (nh3) là (nh4)2so4
phương trình:
Na2so4+ba(oh)2 -> baso4 (kết tủa trắng) + 2naoh
2nh4cl + ba(oh)2 -> bacl2 + 2nh3(bay hơi, mùi khai ) + 2h2o
(nh4)2so4 + ba(oh)2 -> baso4 (kt) + 2nh3(bay hơi) + 2h2o

Để phân biệt các dung dịch: NH3, Na2SO4, NH4Cl, (NH4)2SO4, có thể dùng thuốc thử lần lượt là: dd BaCl2, dd NaOH.

Đặt x là số mol của NH4Cl ta đã có NH4Cl :(NH4)2SO4 =1:2 => (NH4)2SO4 là 2x
NH4Cl + NaOH --(t°)---> NaCl + NH3 + H2O
x ----------- -------------- ------------ ---> x (mol)
(NH4)2SO4 + 2NaOH --(t°)---> Na2SO4 + 2NH3 + 2H2O
2x ------ ------------- ----------- ------- ------ --------> 4x (mol)
n NH3 = 13,44 / 22,4 = 0,6 (mol)
Dựa vào pt :
=> x + 4x = 0,6
<=> 5x = 0,6
<=> x = 0,12 (mol)
=> n NH4Cl = 0,12 (mol)
=> n (NH4)2SO4 = 0,24 (mol)
=> m NH4Cl = 0,12 . 53,5 = 6,42 (g)
=> m (NH4)2SO4 = 0,24 . 132 = 31,68 (g)
=> m A = 6,42 + 31,68 = 38,1 (g)
NH4Cl + NaOH --(t°)---> NaCl + NH3 + H2O
x ----------- -------------- ------------ ---> x (mol)
(NH4)2SO4 + 2NaOH --(t°)---> Na2SO4 + 2NH3 + 2H2O
2x ------ ------------- ----------- ------- ------ --------> 4x (mol)
n NH3 = 13,44 / 22,4 = 0,6 (mol)
Dựa vào pt :
=> x + 4x = 0,6
<=> 5x = 0,6
<=> x = 0,12 (mol)
=> n NH4Cl = 0,12 (mol)
=> n (NH4)2SO4 = 0,24 (mol)
=> m NH4Cl = 0,12 . 53,5 = 6,42 (g)
=> m (NH4)2SO4 = 0,24 . 132 = 31,68 (g)
=> m A = 6,42 + 31,68 = 38,1 (g)

Phương trình phân tứ và ion xảy ra trong dung dịch :
a) Fe2(SO4)3 + 6NaOH → 2Fe(OH)3↓ + 3Na2SO4
2Fe3+ + 3SO42- + 6Na+ + 6OH- → 2Fe(OH)3↓+ 6Na+ + 3SO42-
Fe3+ + 3OH- → Fe(OH)3↓
b) NH4Cl + AgNO3 → NH4NO3 + AgCl↓
NH4 + Cl- + Ag+ + NO3- → NH4+ + NO3- + AgCl↓
Cl- + Ag+ → AgCl↓
c) NaF + HCl → NaCl + HF↑
Na+ + F- + H+ + Cl- → Na+ + Cl- + HF↑
F- + H+ → HF↑
d) Không có phản ứng xảy ra
e) FeS(r) + 2HCl → FeCl2 + H2S ↑
FeS(r) + 2H+ + 2Cl- → Fe2+ + 2Cl- + H2S↑
FeS(r) + 2H+ → Fe2+ + H2S↑
g) HClO + KOH → KClO + H2O
HClO + K+ + OH- → K+ + CIO- + H2O
HClO + OH- → CIO- + H2O.

Viết các phương trình phân tử và ion rút gọn của các phản ứng (nếu có) xảy ra trong dung dịch giữa các cặp chất sau :
a) Fe2(SO4)3 + 6NaOH -> 3Na2SO4 + 2Fe(OH)3
b) NH4Cl + AgNO3 -> AgCl + NH4NO3
c) NaF + HCl -> NaCl + HF
d) MgCl2 + 2KNO3 -> 2KCl + Mg(NO3)2
e) FeS(rắn) + 2HCl -> FeCl2 + H2S
f) HClO + KOH -> ko có PTHH

a/ Fe2(SO4)3 + 6NaOH----> 2Fe(OH)3 + 3Na2SO4
Fe3+ + 3OH- -----> Fe(OH)3
b/ NH4Cl + AgNO3 ------> AgCl + NH4NO3
Cl- + Ag+ -----> AgCl
c/ NaF + HCl -----> HF + NaCl
F- + H+ ------> HF
d/ khong xay ra
e/ FeS + 2HCl -----> FeCl2 + H2S
FeS + 2H+------> Fe2+ + H2S
f/ HClO + KOH -----> KClO + H20
HClO + OH- -----> ClO- + H2O
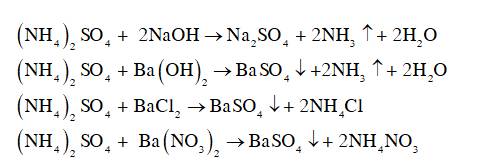
tham khảo.
Hiện tượng: Khi đun nóng dung dịch muối ammonium với NaOH đặc, xuất hiện khí có mùi khai, xốc. Đặt mẩu quỳ tím ẩm lên miệng ống nghiệm, quỳ tím hóa xanh.
Giải thích: Khi đun nóng dung dịch muối ammonium với NaOH đặc, sinh ra khí ammonia có mùi khai, xốc. Khí ammonia tiếp xúc với nước trong quỳ tím ẩm, ammonia nhận H+ của nước, tạo thành ion ammonium (), dung dịch có tính base yếu, làm giấy quỳ tím hóa xanh.