
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án C
+ Bảo toàn nguyên tố cacbon ta có: 2CH4 → CH2=CHCl.
+ Ta có mPVC = 1000 kg ⇒ nPVC = 16 kmol.
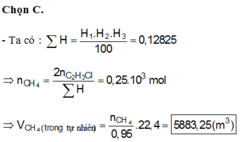
Ta có hiệu suất tổng = 0,15 × 0,95 × 0,9 = 0,12825.
⇒ nCH4 cần dùng = 16 × 2 ÷ 0,12825 ≈ 249,51 kmol.
⇒ VKhí thiên nhiên cần dùng = (249,51 ÷ 0,95) × 22,4 ≈ 5883m3

a) Nhiệt lượng cần để để đun nóng 100 lít nước từ 20oC lên 100oC
[4,18x(100 – 20).105 = 334.105 (J) = 334.102 KJ.
Gọi số mol khí thiên nhiên là x mol.
Vậy: số mol CH4 là 0,85x mol; số mol C2H6 là 0,1x mol.
Do đó: 0,85x mol CH4 tỏa ra nhiệt lượng là: 880 x 0,85x = 748 (kJ).
0,1x mol C2H6 tỏa ra nhiệt lượng là 1560 x 0,10x = 156x (kJ).
Ta có: 748x + 156x = 334x102 => x = 36,9 mol.
Vậy, thể tích khí thiên nhiên cần dùng để đun nóng 100 lít nước từ 20oC lên 100oC là 22,4x = 827 lít.
b) 827 lít khí thiên nhiên có 0,85x mol CH4 và 0,1x mol C2H6
106 lít khí thiên nhiên có a mol CH4 và b mol C2H6.
a = = 3,79x104 (mol) CH4
b = = 4,46.103 (mol) C2H6.
2C2H4 → C2H2 → C2H3Cl
2 mol 1mol
3,79.104 mol 1,9.104 mol
C2H6 → C2H2 → C2H3Cl
1 mol 1 mol
4,46.103 mol 4,46.103 mol
Số mol C2H3Cl thực tế thu được:
(1,9.104 + 4,46.103)x0,65 = 1,52.104 (mol)
Khối lượng C2H3Cl thực tế thu được:
1,52.104 x 62,5 = 95.104 (g) = 950 kg.

Đáp án A
Giải:
A là C2H2 , B là CH2=CHCl
Thể tích khí thiên nhiên (đktc) cần là :
V = 1.1000/62,5.2.22,4:90%:95%:15%;95%=5883 m3 => Đáp án A
Thể tích khí thiên nhiên (đktc) cần là : V = 1.1000/62,5.2.22,4:90%:95%:15%;95%=5883 m3

Sơ đồ phản ứng : 2nCH4 → nC2H2 → nC2H3Cl→ (-CH2-CHCl-)n
Cứ (16.2n) g CH4 tạo ra (62, 5.n) g PVC theo lý thuyết
=> Để tạo 1 tấn PVC cần 0,512 tấn CH4
Mà H = 20% => Khối lượng CH4 thực tế phải dùng là : 2,56 tấn
=> nCH4 = 0,16 tấn mol => nKhí thiên nhiên = 0,188 tấn mol
=> V = 4216,47 m3
=>D