

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



a)
\(\overline{NTK}_{Ag}=107,88\\ \Leftrightarrow\dfrac{109.44\%+A_2.56\%}{100\%}=107,88\\ \Leftrightarrow A_2=107\left(đ.v.C\right)\)
b)
\(\overline{NTK}_B=10,812\\ \Leftrightarrow\dfrac{10.18,8\%+A_2.81,2\%}{100\%}=10,812\\ \Leftrightarrow A_2=11\left(đ.v.C\right)\)

Nguyên tử khối trung bình A của nguyên tố bo trong tự nhiên :
![]()
Nguyên tử khối trung bình của nguyên tố bo : 10,8.

\(a,\\ Đặt:\%^{10}B=a\\\%^{11}B=100\%-a\\ \overline{A}_B=10,812\\ \Leftrightarrow\dfrac{10a+11\left(100\%-a\right)}{100\%}=10,812\\ \Leftrightarrow a=18,8\%\\ \Rightarrow\%^{10}B=18,8\%;\%^{11}B=81,2\%\)
\(b,\\ Đặt:\%^{12}C=a\\ \%^{13}C=100\%-a\\ \overline{A}_C=12,011\\ \Leftrightarrow\dfrac{12a+13.\left(100\%-a\right)}{100\%}=12,011\\ \Leftrightarrow a=98,9\%\\ \Rightarrow\%^{12}C=98,9\%;\%^{13}C=1,1\%\)

Đáp án D
• Giả sử % nguyên tử 11B và 10B trong tự nhiên lần lượt là x, y.
Ta có hpt:
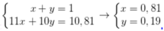
Nếu có 1539 nguyên tử 10B thì có
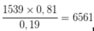 nguyên tử 11B.
nguyên tử 11B.

\(a,\overline{NTK}_B=\dfrac{10.18,89\%+11.81,11\%}{100\%}=10,8111\left(đ.v.C\right)\\ b,\overline{NTK}_{Ne}=\dfrac{20.91\%+22.\left(100\%-91\%\right)}{100\%}=20,18\left(đ.v.C\right)\\ c,\overline{NTK}_{Br}=\dfrac{79.54,5\%+81.\left(100\%-54,5\%\right)}{100\%}=79,91\left(đ.v.C\right)\\ d,\overline{NTK}_{Mg}=\dfrac{24.78,99\%+25.10\%+26.\left(100\%-78,89\%-10\%\right)}{100\%}\\ =24,3202\left(đ.v.C\right)\)
\(e,\overline{NTK}_{Ar}=\dfrac{36.0,34\%+38.0,06\%+40.\left(100\%-0,34\%+0,06\%\right)}{100\%}\\ =39,9852\left(đ.v.C\right)\\ f,\overline{NTK}_{Fe}=\dfrac{54.5,84\%+56.91,68\%+57.2,17\%+58.0,31\%}{100\%}\\ =55,9111\left(đ.v.C\right)\)

Đáp án A
Giả sử % 10B và % 11B trong tự nhiên lần lượt là x, y.
Ta có hpt:
![]()
Vậy phần trăm số nguyên tử đồng vị 10B trong H3BO3 là
![]()