Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PTHH: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
a+b) \(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Fe_2O_3}=0,2\left(mol\right)\\n_{H_2}=0,6\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Fe_2O_3}=0,2\cdot160=32\left(g\right)\\V_{H_2}=0,6\cdot22,4=13,44\left(l\right)\end{matrix}\right.\)
c) PTHH: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\uparrow\)
Theo PTHH: \(n_{Zn}=n_{H_2}=0,6\left(mol\right)\)
\(\Rightarrow m_{Zn}=0,6\cdot65=39\left(g\right)\)
a,
nFe = 22,4/56 = 0,4 (mol)
PTHH
Fe2O3 + 3H2 ---to----) 2Fe + 3H2O (1)
theo phương trình (1) ,ta có:
nFe2O3 = 0,4 x 2 / 1 = 0,8 (mol)
mFe2O3 = 160 x 0,8 = 128 (g)
b,
theo pt (1)
nH2 = (0,4 x 3)/2 = 0,6 (mol)
=) VH2 = 0,6 x 22,4 = 13,44 (L)
c,
PTHH
Zn + H2SO4 -------------) ZnSO4 + H2 (2)
Số mol H2 cần dùng là 0,6 (mol)
Theo PT (2) :
nZn = nH2 ==) nZn = 0,6 x 65 = 39 (g)

a)
\(n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)\\ Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O\\ n_{Fe_3O_4} = \dfrac{1}{3}n_{Fe} = \dfrac{1}{15}(mol)\\ \Rightarrow m_{Fe_3O_4} = \dfrac{1}{15}.232 = 15,467(gam)\)
b)
\(n_{H_2} = \dfrac{4}{3}n_{Fe} = \dfrac{4}{15}(mol)\\ \Rightarrow V_{H_2} =\dfrac{4}{15}.22,4 = 5,973(lít)\)
\(n_{Fe}=\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
PTHH: \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
...............1...............4..............3.....................
...............1/15.........4/15.........0,2..................
a. \(m_{Fe_3O_4}=n_{Fe_3O_4}\cdot M_{Fe_3O_4}=\dfrac{1}{15}\cdot232=\dfrac{232}{15}\left(g\right)\)
b. \(V_{H_2\left(ĐKTC\right)}=n_{H_2}\cdot22,4=\dfrac{4}{15}\cdot22,4=\dfrac{448}{75}\left(l\right)\)

\(n_{Fe}=\dfrac{2,8}{56}=0,05mol\)
\(\Rightarrow m_{Cu}=6-2,8=3,2g\)\(\Rightarrow n_{Cu}=0,05mol\)
\(CuO+H_2\rightarrow Cu+H_2O\)
0,05 0,05
\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
0,075 0,05
\(\Rightarrow\Sigma n_{H_2}=0,075+0,05=0,125mol\)
\(\Rightarrow V=0,125\cdot22,4=2,8l\)

\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: Fe2O3 + 3H2 --to--> 2Fe + 3H2O
0,1 0,3 0,2
\(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: 3Fe + 2O2 --to--> Fe3O4
LTL: \(\dfrac{0,2}{3}>\dfrac{0,1}{2}\rightarrow\) Fe dư
Theo pthh: \(n_{Fe\left(pư\right)}=\dfrac{3}{2}n_{O_2}=\dfrac{3}{2}.0,1=0,15\left(mol\right)\)
\(\rightarrow m_{Fe\left(dư\right)}=\left(0,2-0,15\right).56=2,8\left(g\right)\)
a.\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
0,1 0,3 0,2 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_{O_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\)
\(\dfrac{0,2}{3}\) > \(\dfrac{0,1}{2}\) ( mol )
0,15 0,1 ( mol )
Chất dư là Fe
\(m_{Fe\left(dư\right)}=\left(0,2-0,15\right).56=2,8g\)

Số mol của sắt (III) oxit
nFe2O3 = \(\dfrac{m_{Fe2O3}}{M_{Fe2O3}}=\dfrac{12}{160}=0,075\left(mol\right)\)
Pt : 3H2 + Fe2O3 → 2Fe + 3H2O\(|\)
3 1 2 3
0,225 0,075 0,15
a) Số mol của khí hidro
nH2 = \(\dfrac{0,075.3}{1}=0,225\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,225 . 22,4
= 5,04 (l)
b) Số mol của sắt
nFe= \(\dfrac{0,075.2}{1}=0,15\left(mol\right)\)
Khối lượng của sắt thu được
mFe = nFe . MFe
= 0,15 . 56
= 8,4 (g)
Chúc bạn học tốt
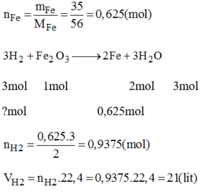
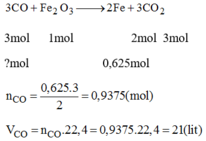

Ta có: \(n_{Fe}=\dfrac{35}{56}=0,625\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=0,9375\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,9375.22,4=21\left(l\right)\)
PT: \(Fe_2O_3+3CO\underrightarrow{t^o}2Fe+3CO_2\)
Theo PT: \(n_{CO}=\dfrac{3}{2}n_{Fe}=0,9375\left(mol\right)\)
\(\Rightarrow V_{CO}=0,9375.22,4=21\left(l\right)\)