Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nAl = 8,1 /27 = 0,3mol
2Al + 6HCl => 2AlCl3 + 3H2
0,3--------------->0,3------> 0,45
=> VH2 = 0,45.22,4 = 10,08 (l)
mAlCl3 = 0,3. 133,5 = 40,05 (g)

a.\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72\left(l\right)\)
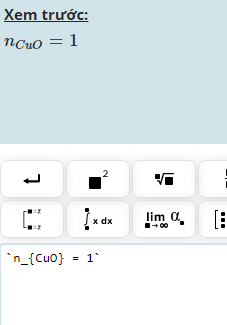
b.\(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
\(CuO+H_2\rightarrow\left(t^o\right)Cu+H_2O\)
0,6 > 0,3 ( mol )
0,3 0,3 ( mol )
\(m_{Cu}=0,3.64=19,2\left(g\right)\)
c.\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\)
0,3 0,15 ( mol )
\(V_{kk}=V_{O_2}.5=\left(0,15.22,4\right).5=16,8\left(l\right)\)

\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
a) 2Al + 6HCl --> 2AlCl3 + 3H2
b) \(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
2Al + 6HCl --> 2AlCl3 + 3H2
\(\dfrac{0,4}{3}\)<--------------------0,2
=> Al dư
\(m_{Al\left(dư\right)}=\left(0,2-\dfrac{0,4}{3}\right).27=1,8\left(g\right)\)

\(n_{Mg}=\dfrac{2,4}{24}=0,1\left(mol\right);n_{HCl}=\dfrac{3,65}{36,5}=0,1\left(mol\right)\\ a,Mg+2HCl\rightarrow MgCl_2+H_2\\ Vì:\dfrac{0,1}{2}< \dfrac{0,1}{1}\\ \Rightarrow Mgdư\\ \Rightarrow n_{Mg\left(p.ứ\right)}=n_{MgCl_2}=n_{H_2}=\dfrac{0,1}{2}=0,05\left(mol\right)\\ n_{Mg\left(dư\right)}=0,1-0,05=0,05\left(mol\right)\\ \Rightarrow m_{Mg\left(dư\right)}=0,05.24=1,2\left(g\right)\\ b,m_{MgCl_2}=95.0,05=4,75\left(g\right)\\ c,V_{H_2\left(đktc\right)}=0,05.22,4=1,12\left(l\right)\)

a) PTHH: 2Al + 6HCl ===> 2AlCl3 + 3H2
b) nAl = \(\frac{27}{27}=1\left(mol\right)\)
Theo phương trình, nAlCl3 = nAl = 1 (mol)
=> Khối lượng AlCl3 tạo thành: mAlCl3 = 1 x 133,5 = 133,5 gam
a) Al + HCl \(\rightarrow\) AlCl + H2
b) Áp dụng ĐLBTKL
mAl + mHCl= mAlCl + mH

2Al+6HCl->2AlCl3+3H2
0,05----0,15------------------0,075 mol
n H2=\(\dfrac{1,68}{22,4}\)=0,075 mol
=>m Al=0,05.27=1,35g
=>HCl dư =>m HCl=0,1.36,5=3,65g

nAl=0,2mol
PTHH: 2Al+6HCl=>2AlCl3+3H2
0,2->0,6-> 0,2--->0,3
mAlCl3=0,2.133,5=26,7g
do H=90
=> mAlCl3=26.7/100.90=24,03g
VH2=0,3.22,4=6,72l
do H=90%
=> V H2=6,72/100.90=6,048l
nAl=5,4/27=0,2(mol)
voi h=90->nAl=0,2*90/100=0,18(mol)
2Al+6HCl->2AlCl3+3H2
TPT;nAlCl3=3nAl=0,18*3=0,54(mol)
->mAlCl3=0,54*133,5=72,09(g)
TPT;nH2=3/2nAl=0,18*3/2=0,12(mol)
->VH2=0,12*22,4=2,688(l)
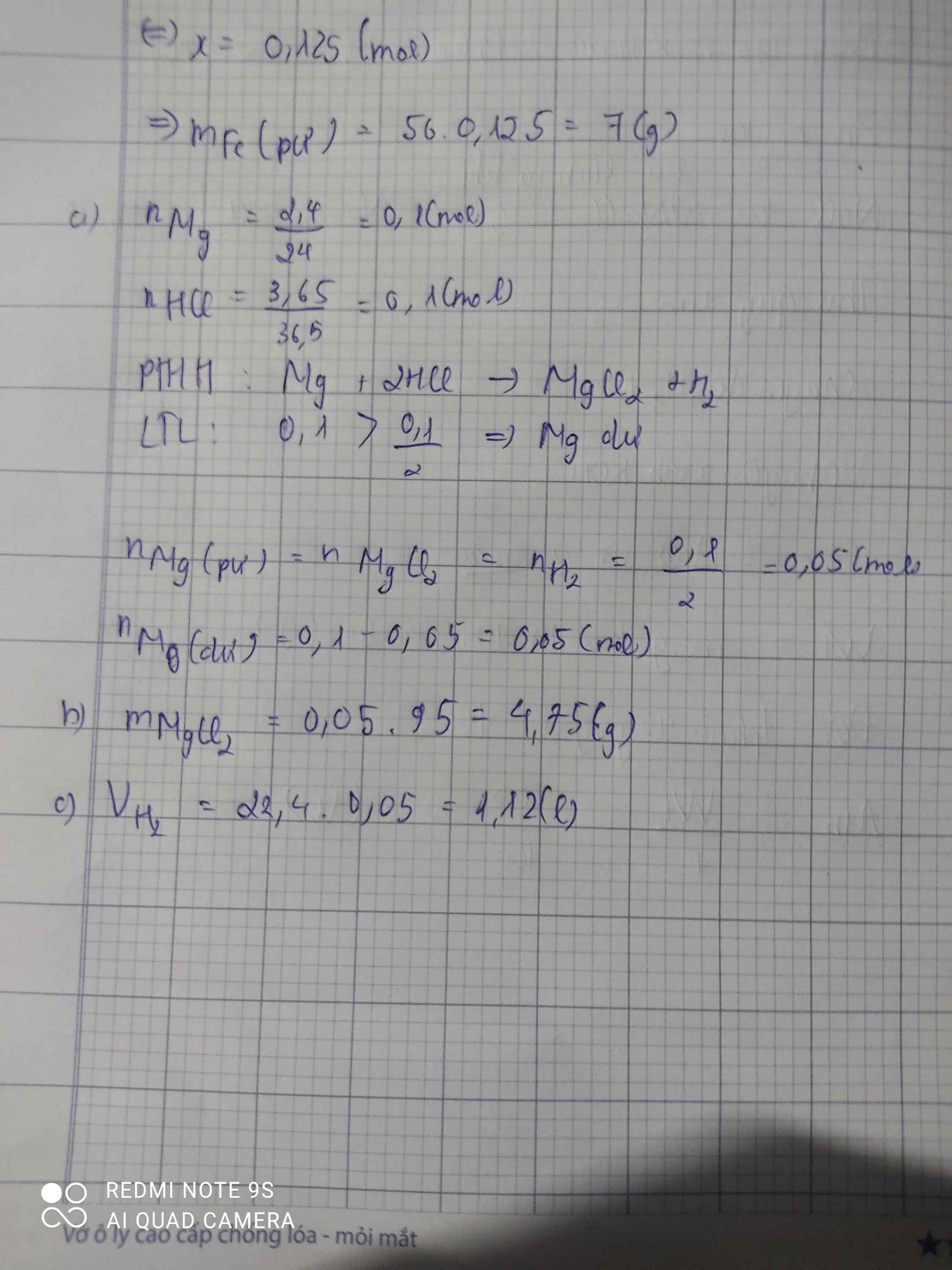
a: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(n_{HCl}=\dfrac{10.95}{36.5}=0.3\left(mol\right)\)
Vì \(\dfrac{0.2}{2}>\dfrac{0.3}{6}\) nên Al dư và dư 0,05 mol
b: \(n_{AlCl_3}=0.9\left(mol\right)\)
\(m_{AlCl_3}=0.9\cdot136.5=122.85\left(g\right)\)