Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nFe = \(\frac{11,2}{56}=0,2mol\)
nAl = \(\frac{m}{27}mol\)
Cốc A : Fe + 2HCl -> FeCl2 + H2
0,2 0,2
Theo định luật bảo toàn khối lượng khối lượng HCl tăng thêm;
11,2 - 0,2.2 = 10,8 g
Cốc B : 2Al + 3H2SO4 -> Al2(SO4)3 + 2H2
\(\frac{m}{27}\) \(\frac{3m}{27.2}\)
Khi cho mg Al vào cốc B thì cốc B tăng thêm là ;
m - \(\frac{3m}{27.2}\).2 = 10,8
=> m = 12,15 g

\(n_{Fe}=\dfrac{11,2}{56}=0,2mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,2 0,2
\(\Rightarrow m_{Fe}+m_{H_2SO_4}=0,2\cdot56+0,2\cdot98=30,8g\)
Cả hai đĩa cân thăng bằng:
\(m_{Fe}+m_{H_2SO_4}=m_{Al}+m_{H_2SO_4}\)
\(\Rightarrow m_{Fe}=m_{Al}=11,2g\)

\(Fe + 2HCl \to FeCl_2 + H_2\\ n_{H_2} = n_{Fe} = \dfrac{11,2}{56} =0,2(mol)\\ \Rightarrow m_{tăng} = 11,2 - 0,2.2 = 10,8(gam)\\ 2Al +3 H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ n_{Al} = \dfrac{m}{27}(mol)\\ \Rightarrow n_{H_2} = \dfrac{3}{2}n_{Al} = \dfrac{m}{18}(mol)\)
Vì cân ở vị trí thăng bằng nên :
\(m - \dfrac{m}{18}.2 = 10,8\Rightarrow m =12,15(gam)\)

Fe + 2HCl → FeCl2 + H2
Theo PTHH :
n H2 = n Fe = 11,2/56 = 0,2(mol)
=> m tăng = m Fe - m H2 = 11,2 - 0,2.2 = 10,8(gam)
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
n Al = m/27
n H2 = 3/2 n Al = m/18(mol)
=> m tăng = m Al - m H2 = m - m/18 . 2 = 8m/9(gam)
Vì cân thăng bằng nên : 10,8 = 8m/9
=> m = 12,15 (gam)

Câu hỏi của Dịch Thiên Tổng - Hóa học lớp 8 | Học trực tuyến

Em ơi đề hơi kì nha, cốc A đựng dd HCl, cốc B đựng dd H2SO4 vậy cốc ở đâu đựng nước?
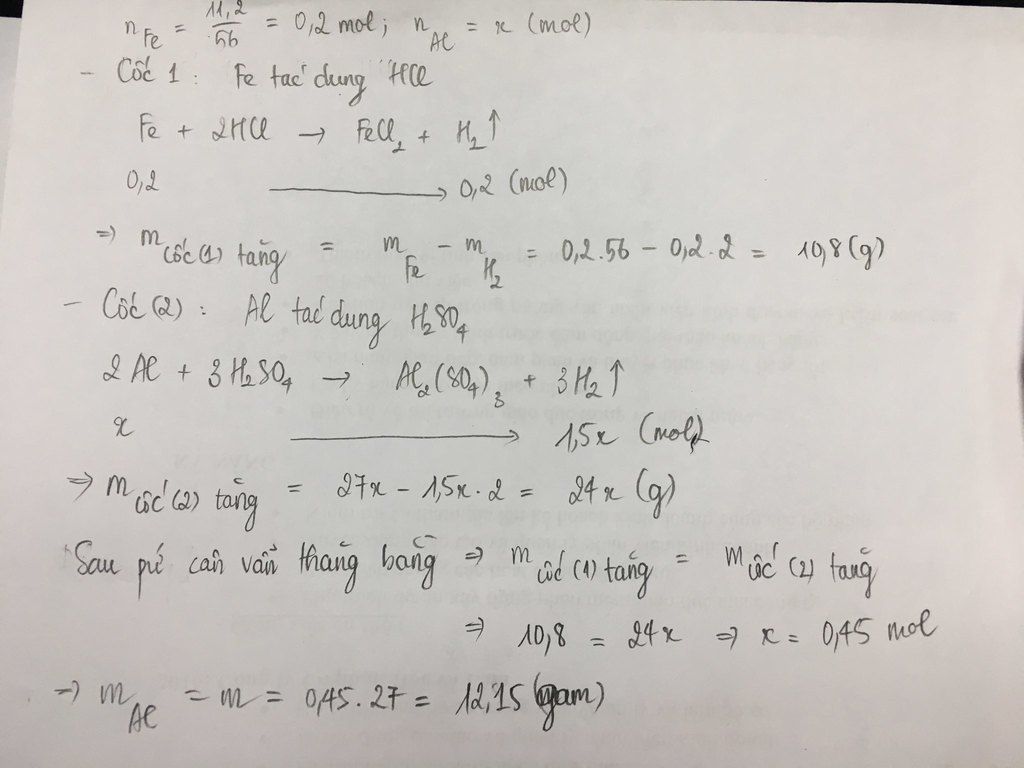

\(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
\(n_{Al}=\dfrac{m}{27}\left(mol\right)\)
Fe + 2HCl -> FeCl2 + H2\(\uparrow\)
0,2________________0,2 (mol)
=> nH2 = 0,2 (mol) => mH2 = 0,2.2 = 0,4 (gam)
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2
\(\dfrac{m}{27}...........................\dfrac{m}{18}\)(mol)
\(\Rightarrow n_{H2}=\dfrac{m}{18}\Rightarrow m_{H2}=\dfrac{m}{18}.2=\dfrac{m}{9}\left(gam\right)\)
Khối lượng của đĩa đựng HCl tăng là :
11,2 - 0,4 = 10,8 (gam)
Khối lượng đĩa đựng H2SO4 là:
\(m-\dfrac{m}{9}=\dfrac{8m}{9}\left(gam\right)\)
Theo bài 2 đĩa thăng bằng nên ta có
\(10,8=\dfrac{8m}{9}\Rightarrow m=12,5\left(gam\right)\)
nFe=m/M=11,2/56=0,2(mol)
nAl=\(\dfrac{m}{27}\)(mol)
PT1:
Fe + 2HCl -> FeCl2 + H2\(\uparrow\)
1..........2............1............1 (mol)
0,2-> 0,4 -> 0,2 -> 0,2 (mol)
=> mH2=n.M=0,2.2=0,4 (gam)
PT2:
2Al + 3H2SO4 -> Al2(SO4)3 + 3H2\(\uparrow\)
2..............3....................1....................3 (mol)
\(\dfrac{m}{27}\) ................................................> \(\dfrac{m}{18}\left(mol\right)\)
=> mH2=n.M=\(\dfrac{m}{18}.2=\dfrac{m}{9}\left(g\right)\)
từ đó ,ta được
mHCl=11,2 - 0,4 =10,8 (gam)
mH2SO4=m - \(\dfrac{m}{9}=\dfrac{8m}{9}\) (gam)
Theo bài 2 đĩa cân bằng nên:
10,8=\(\dfrac{8m}{9}\)
\(\Leftrightarrow97,2=8m\)\(\Rightarrow m=12,15\left(gam\right)\)