Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Fe_2O_3}=n_{FeO}=n_{Fe_3O_4}=a\\ n_{NO_2}:n_{NO}=\dfrac{46-34}{34-30}=3\\ n_{NO_2}+n_{NO}=\dfrac{4,48}{22,4}=0,2\\ n_{NO_2}=0,15;n_{NO}=0,05\\ BTe:a+a=0,15+0,15\\ a=0,15\\ m_A=a\left(160+232+72\right)=69,6g\\ BT\left[N\right]:V_{HNO_3}=\dfrac{6a\cdot3-0,2}{2}=1,25L\)

nN2 = nNO2 => Quy đổi N2 và NO2 thành N3O2 và quy N3O2 về N2O và NO. Vậy ta giả sử rằng hỗn hợp N2,N2O,NO,NO2 sau khi quy đổi thì có 2 khí là NO và N2O. ĐẶt số mol a,b tương ứng cho NO và N2O
------------3a---------a
2N+5+2.4e=>2N+1
--------------8b-------2b

Ta có :
\(M_A=\frac{m_{NO}+m_{N_2O}}{n_{NO}+n_{N_2O}}=16,75.2=33,5\)
<=> \(33,5=\frac{30n_{NO}+44n_{N_2O}}{n_{NO}+n_{N_2O}}\)
<=> \(3,5n_{NO}=10,5n_{N_2O}\)
=> \(n_{NO}=3n_{N_2O}\)
Lại có
Al0+ ----> -3e Al3+ N5+----> +3e N2+
0,17_____0,51__0,17 3a______9a____3a
2N5+----> +8e 2N1+
a_______8a____a
=> \(n_{Al}=\frac{4,59}{27}=0,17\left(mol\right)\)
Gọi a là số mol của \(N_2O\)
=> 3a___________NO
=> 9a+8a=0,51
=>a=0,03(mol)
a)=> Σnh2=0,03+0,03.3=0,12(mol)
=> Vh2=0,12.22,4=2,688(l)
b)\(M_B=16,4.2=32,8\left(\frac{gam}{mol}\right)\)
<=> \(\frac{44n_{N_2O}+30n_{NO}}{n_{N_2O}+n_{NO}}=32,8\)
<=>11,2\(n_{N_2O}\)=2,8\(n_{NO}\)
=> \(n_{NO}=4n_{N_2O}\)
mà trước khi trộn : \(n_{NO}=3n_{N_2O}\)
=> trộn thêm số mol khí \(n_{NO}=n_{N_2O}=0,03\left(mol\right)\)
=> \(V_{NO}=0,03.22,4=0,672\left(mol\right)\)

hỗn hợp 2 oxit thu được gồm 2 oxit nên Al tan hết và 1 phần Fe đã pư
gọi x là số mol của Al
2Al + 3CuSO4 --> Al2(SO4)3 + 3Cu
x_____3x/2_______x/2________3x/2
Fe + CuSO4 --> FeSO4 + Cu
0,04-3x/2__0,04 - 3x/2 __0,04 - 3x/2
Al2(SO4)3 -----------> 2Al(OH)3 ---------Al2O3
---------------------------------------... x/2 mol
2FeSO4 ----------------> 2Fe(OH)2 --------> 2Fe(OH)3 ---------> Fe2O3
0,04 - 3x/2------------------------------------... (0,04 - 3x/2)/2
Khối lượng 2 oxit:
102*x/2 + 160*(0,04 - 3x/2)/2 = 1,82 --> giải ra ta được x = 0,02 mol
gọi a và b lần lượt là số mol của Fe và Cu trong D
cho D tác dụng với dung dịch AgNO3:
Fe + 2AgNO3 --> Fe(NO3)2 + 2Ag
a--------------------------------------... 2a
Cu + 2AgNO3 --> Cu(NO3)2 + 2Ag
b--------------------------------------... 2b
--> 108*2*(a+b) - (56a + 64b) = 7,336 (1)
Tổng khối lượng của hỗn hợp A là 1,572g
27*0,02 + 56(a + 0,01) + 64*(b - 0,04) = 1,572 (2)
Giải hệ (1) và (2) ta sẽ thu được kết quả a và b

hòa tan hoàn toàn khối lượng Fe và Cu(tỉ lệ 1:1) bằng axit HNO3 thu được V lít hỗn hợp khí X gồm NO và NO2 và dung dịch Y (chỉ chứa 2 muốivà axit ) tỉ khối của X đối với H2 bằng 19. tính V
các bạn giải theo cách bảo toàn electron nha
a) Ta có: nH2 = 1,008/22.4 = 0,045 \(\rightarrow\) nHCl = 0,045 x 2= 0,09mol
mA = mmuối - mCl = 4,575 - 0,09 x 35,5 = 1,38g
Đặt x, y lần lượt là số mol của Fe, M và n là hóa trị của M trong hợp chất. Từ 2 phương trình ta có:
56x + My = 1,38 (1)
2x + ny = 0,09 (2)
b) Ở câu b này mình cho rằng đó là H2SO4 đặc chứ ko phải loãng vì nếu loãng thì ta ko thu được hh khí có tỉ khối hơi như vậy.
Các phương trình phản ứng:
Fe + 6HNO3 \(\rightarrow\) Fe(NO3)3 +3NO2 + 3H2O
M + 2nHNO3\(\rightarrow\) M(NO3)n + nNO2 + nH20
2Fe + 6H2SO4 \(\rightarrow\) Fe2(SO4)3 + 3SO2 + 6H2O
2M + 2nH2SO4 \(\rightarrow\) M2(SO4)n + nSO2 + 2nH2O
Ta có: dkhí/ H2 =25,25 \(\rightarrow\) Mkhí = 50,5
Số mol 2 khí=1,8816:22,4=0,084mol
lập hệ giải ra: nNO2 = 0,063, nSO2 = 0,021
Ta có các phương trình e như sau:
Fe \(\rightarrow\) Fe3+ + 3e
x---------------3x
M \(\rightarrow\) Mn+ + ne
y--------------ny
N5+ + 1e \(\rightarrow\) N4+
0,063 \(\leftarrow\) 0,063
S6+ + 2e\(\rightarrow\) S4+
0,042 \(\leftarrow\) 0,021
Tổng e nhận = tổng e nhường nên :
3x + ny = 0,063 + 0,042 = 0,105
kết hợp với (2) suy ra được x = 0,015
ny = 0,06 \(\rightarrow\) y = 0,06/n
Thay vào (1) \(\rightarrow\) M = 9n
Biện luận thì tìm được M là Al.

\(Al\left(x\right)+4HNO_3\rightarrow2H_2O+NO\left(x\right)+Al\left(NO_3\right)_2\)
\(8Al\left(\frac{8y}{3}\right)+30HNO_3\rightarrow15H_2O+3N_2O\left(y\right)+8Al\left(NO_3\right)_2\)
Gọi số mol NO, N2O lần lược là x, y
\(n_{Al}=\frac{4,59}{27}=0,17\)
\(\Rightarrow x+\frac{8y}{3}=0,17\left(1\right)\)
\(M_{hh}=16,75.2=33,5\)
\(\Rightarrow\frac{30x+44y}{x+y}=33,5\)
\(\Leftrightarrow x=3y\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{\begin{matrix}x+\frac{8y}{3}=0,17\\x=3y\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}x=0,09\\y=0,03\end{matrix}\right.\)
\(\Rightarrow V_{NO}=0,09.22,4=2,016\)
\(\Rightarrow V_{N_2O}=0,03.22,4=0,672\)

1)
nNO3(-) trong muối = nNO2 + 3nNO + 8nN2O + 10nN2 = x + 3y + 8z + 10t
m muối = m kim loại + mNO3(-) = a + 62.(x + 3y + 8z + 10t)
vậy chọn đáp án A
2)
nNO3(-) trong muối = 62g => nNO3(-) = 1mol
2Cu(NO3)2 => 2CuO + 4NO2 + O2
4Fe(NO3)3 => 2Fe2O3 + 12NO2 + 3O2
Zn(NO3)2 => 2ZnO + 4NO2 + O2
nNO2 = nNO3(-) = 1 mol
nO2 = nNO2/4 = 1/4 = 0,25mol
=> m chất rắn = m + 62 - 46 - 32.0,25 = m + 8
vậy chọn đáp án A

nFe = 0,1 mol. m O2 = 7,36 - 5,6 = 1,76 gam => n O2 = 0,055 mol
Đặt nNO = x, nNO2 = y
Ta có hệ: bảo toàn electron: 3.0,1 - 0,055.4 = 3x + y
30x + 44y / ( x+y) = 19.2
=> x= 0,02, y =0,02
=> V = 0,04.22,4 = 8,96 lít
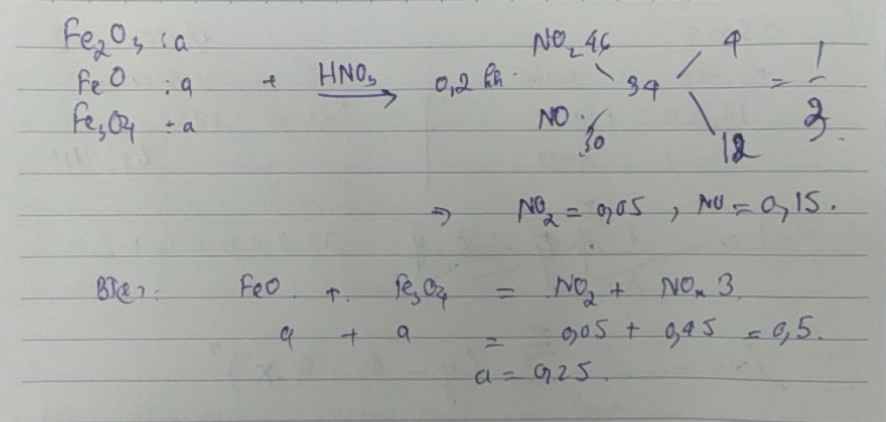
giúp vs ạ