Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn đáp án A
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n C u = n S O 2 = 0 , 075 m o l
Đặt nCr = x mol; nFe = y mol ⇒ m X = 52x + 56y + 0,075 × 64 = 18,2 gam.
nH2 = x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
⇒ % mCr trong X = 42,86% và %mCu trong X = 26,37%

Đáp án : A
nH2 = 0,25 mol; nSO2 = 0,3 mol
2H+ + 2e → H2 S+6 + 2e → S+4
0,5 <-- 0,25 0,6 <-- 0,3
nFe = 0,6 – 0,5 = 0,1 mol
=> mFe = 5,6g

Đáp án : B
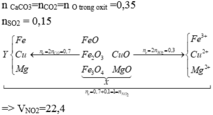
nCO2 = nO pứ =nCaCO3 = 0,15 mol
nH2SO4 = 0,35 mol ; nH2 = 0,05 mol
Bảo toàn H : nH2SO4 = nH2 + nH2O => nH2O = 0,3 mol = nO (oxit)
=> nO bđ =0,3 + 0,15 = 0,45 mol
=> 3nAl2O3 + 3nFe2O3 = 0,45 mol
Và 102nAl2O3 + 160nFe2O3 = 21,1g
=> nAl2O3 = 0,05 mol ; nFe2O3 = 0,1 mol
=> %mAl2O3 = 24,17%

Định hướng tư duy giải
→ n NH 4 + = 0 , 235 . 2 - 0 , 14 . 3 8 = 0 , 00625
=> 110,23 = 0,73943m + 96.(0,235+0,26057m/16) => m = 38,07
=> mY = 28,15 + 62.(0,00625.8 + 0,14.3 + 0,62.2) + 80.0,00625 = 134,67
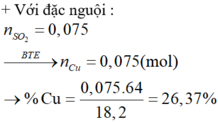
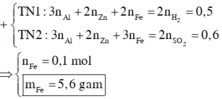


a) Fe + H2SO4 ---> FeSO4 + H2
Al2O3 + 3H2SO4 ---> Al2(SO4)3 + 3H2O
nFe = nH2 = 11,2/22,4 = 0,5 mol. ---> mFe = 56.0,5 = 28g; mAl2O3 = 40 - 28 = 12g.
b) 2Fe + 6H2SO4 ---> Fe2(SO4)3 + 3SO2 + 6H2O
Al2O3 + 3H2SO4 ---> Al2(SO4)3 + 3H2O
nSO2 = 1,5nFe = 1,5.0,5 = 0,75 mol.
V = 0,75.22,4 = 16,8 lít.