Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

lớp e : (1s)(2s2p)(3s3p3d)(4s4p4d4f)....
câu a : NT X có 3 lớp e => 1s2s2p3s3p3d
vì có 5 e lớp ngoài cùng => C/h e : 1s22s22p63s23p3
câu b, c tương tự nhé

1. C
2. C
3. C
4. B
5. A
6. C
7. B
8. Cation M mang -3 hay +3 hả bạn ơi
1. Nguyên tử nguyên tố X có 1e lớp ngoài cùng và có tồng số e ở phân lớp d và p là 17. Số hiệu của X là:
A. 29 B. 24 C. 25 D. 19
2. Cấu hình electron của ion nào sau đây không giống cấu hình của khí hiếm:
A. Cl B. Mg2+ C. S2- D. Fe3+
3. Một nguyên tử X có tổng số electron ở các phân lớp p là 11. Nguyên tố X thuộc loại:
A. nguyên tố d B. nguyên tố s C. nguyên tố p D. nguyên tố f
4. Nguyên tử của nguyên tố A và B đều có phân lớp ngoài cùng là 2p. Tổng số e ở hai phân lớp ngoài cùng hai nguyên tử này là 3. Vậy số hiệu nguyên tử của A và B lần lượt là:
A. 1&2 B. 5&6 C. 7&8 D. 7&9
5. Biết các electron của nguyên tử lưu huỳnh được phân bố trên 3 lớp electron (K, L, M) lớp ngoài cùng có 6 electron. Số electron ở lớp L trong nguyên tử lưu huỳnh là:
A. 8 B. 6 C. 10 D. 12
6. Nguyên tử R tạo cation R+. Cấu hình e của R+ ở trạng thái cơ bản là 3p6. Tổng số hạt mang điện trong R là:
A. 18 B. 22 C. 38 D. 19
7. Cấu hình e nào sau đây đúng:
A. [Ar}3d34s2 B. [Ar]3d64s2 C. [Ar]3d64s1 D. [Ar]3d54s1

a) Tổng số electron là 7, suy ra số thứ tự của nguyên tố là 7. Có 2 lớp electron suy ra nguyên tố ở chu kì 2. Nguyên tố p có 5 electron ở lớp ngoài cùng nên thuộc nhóm VA. Đó là ni tơ. Công thức phân tử hợp chất với hidro là NH3
b) Công thức electron và công thức cấu tạo của phân tử NH3
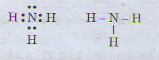

a)
- Tổng số e trên các phân lớp của nguyên tử X là 19 => Nguyên tử X có 19 e
- Tổng số e trên các phân lớp của nguyên tử Y là 16 => Nguyên tử X có 16 e
b)
- Nguyên tử X có 19 e => Nguyên tử X có số hiệu nguyên tử ZX = 19
- Nguyên tử Y có 16 e => Nguyên tử Y có số hiệu nguyên tử ZY = 16
c)
- Trong nguyên tử X lớp electron ở mức năng lượng cao nhất là lớp N (n=4)
- Trong nguyên tử Y lớp electron ở mức năng lượng cao nhất là lớp M (n=3)
d)
- Nguyên tử X có:
+ 4 lớp electron (n = 1, 2, 3, 4)
+ 6 phân lớp electron (gồm 1s, 2s, 2p, 3s, 3p, 4s)
- Nguyên tử Y có:
+ 3 lớp electron (n= 1, 2, 3)
+ 5 phân lớp electron (gồm 1s, 2s, 2p, 3s, 3p)
e)
- Nguyên tử X có 1 e lớp ngoài cùng (4s1) => X là nguyên tố kim loại.
- Nguyên tử Y có 6 e lớp ngoài cùng (3s23p4) => Y là nguyên tố phi kim.

1. c.h.e của X là : \(1s^22s^22p^63s^23p^63d^24s^2\)
tính ta được 22e \(\Rightarrow\)B.22
2.số hiệu nguyên tử =p=e \(\Rightarrow\) B
3. sai đề k bạn tại mình tính ra X là khí hiếm Y là kim loại
Bài 1:
Ta có cấu hình electron của nguyên tố X: \(1s^22s^22p^63s^23p^63d^24s^2\)
Vậy số electron của nguyên tử X là 22
=> Chọn đáp án B
Bài 2:
Cấu hình electron của nguyên tử M là khi Z=11 : \(1s^22s^22p^63s^1\)
Cấu hình electron của nguyên tử M là khi Z=13 : \(1s^22s^22p^63s^23p^1\)
=> Chọn đáp án C
Bài 3:
Cấu hình electron của nguyên tử X: \(1s^22s^22p^63s^23p^6\)
-> X có tính chất của Khí hiếm (vì có 8e ở lớp ngoài cùng)
Cấu hình electron của nguyên tử Y: \(1s^22s^22p^63s^23p^64s^1\)
-> Y có tính chất của Kim loại (vì có 1e ở lớp ngoài cùng
=> Chọn đáp án: Bạn cho đáp án sai -_-
Bài 4:
Nguyên tố X có số hiệu nguyên tử (Z) là 14
Cấu hình electron của X là \(1s^22s^22p^63s^23p^2\)
=> Chọn đáp án A
Bài 5:
Cấu hình electron của Flo: \(1s^22s^22p^5\)
+Tổng hạt electron ở phân lớp s là 4
+Tổng electron lớp ngoài cùng là 7
Cấu hình electron của Lưu huỳnh: \(1s^22s^22p^63s^23p^4\)
+Tổng hạt electron ở phân lớp s là 6
+Tổng electron lớp ngoài cùng 6
Cấu hình electron của Clo: \(1s^22s^22p^63s^23p^5\)
+Tổng hạt electron ở phân lớp s là 6
+Tổng electron lớp ngoài cùng là 7
Cấu hình electron của Oxi: \(1s^22s^22p^4\)
+Tổng hạt electron ở phân lớp s là 4
+Tổng electron lớp ngoài cùng là 6
=> Chọn đáp án B
(*p/s: Ghi sai đề phân lớp s chứ không phải phân lớp X -_-)
Bài 6:
Sai đề -_-! Đề này dịch ko ra @_@
Bài 1:
a. Nguyên tử A:CHE: 1s22s22p63s23p5
Kí hiệu nguyên tố: Cl (Z=17)
b.Nguyên tử B:CHE: 1s22s22p63s23p64s1
Kí hiệu nguyên tố: K (Z=19)